Окислительно-восстановительная активность
Cтраница 1
 |
Стандартные окислительно-восстановительные потенциалы некоторых реакций. [1] |
Окислительно-восстановительная активность изменяется также в зависимости от комплексообразо-вания и строения комплексных ионов. [2]
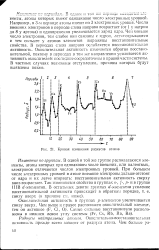 |
Кривая изменения радиусов атомов. [3] |
Окислительно-восстановительная активность прежде всего зависит от радиуса атома. [4]
Окислительно-восстановительная активность гидрокспдов зависит от степени окисления элемента. [5]
Окислительно-восстановительная активность гидроксидов зависит от степени окисления элемента. [6]
Окислительно-восстановительная активность окиси алюминия заметно зависит от температуры активации образца и в меньшей степени от времени активации. [7]
При малом отличии окислительно-восстановительной активности исходных веществ и продуктов реакции процесс является обратимым. [8]
В свете сказанного становится понятным изменение окислительно-восстановительной активности в ряду химических соединений, образованных одним и тем же элементом. С увеличением валентности наблюдается возрастание окислительных свойств с одновременным понижением восстановительной активности; справедливо и обратное утверждение: с уменьшением валентности происходит нарастание восстановительных свойств с одновременным падением окислительной активности. [9]
Окислительно-восстановительный по-тен Диал комплексных соединений, а значит и их окислительно-восстановительная активность, не те, что у исходных ионов. Хорошо известно, что кобальт в трехвалентном состоянии является сильным окислителем. [10]
Если называют химические свойства ( атомный вес, валентность, окислительно-восстановительную активность), то речь идет об элементе. Например, кислород - окислитель и в соединениях двухвалентен. Если кислород двухвалентен, то это значит, что он вошел в состав сложного вещества. В состав сложных веществ простые вещества не входят, а входят атомы элементов. Так, в состав HgO не входят простые вещества жидкая ртуть и газ кислород, а входят атомы элементов ртути и кислорода. [11]
Таким образом, комплексообразование в этой системе под вляет даже окислительно-восстановительную активность реагентов. Повышение устойчивости малостабильных степеней окисления элементов возможно даже за счет образования двойных солей, которые можно рассматривать как комплексные соединения с высокой константой нестойкости. Например, производные Fe ( - f2) неустойчивы в водных растворах по отношению к окислению кислородом воздуха, что создает известные трудности при их изучении. Однако уже в кристаллогидрате FeSO4 7H2O Fe ( - f 2) более стабильно. При этом в растворе могут протекать все реакции, характерные для Fe ( 2), а устойчивость по отношению к кислороду воздуха существенно выше. [12]
От каких свойств атомов зависит их распространение в земной коре и окислительно-восстановительная активность. [13]
Известно, что в ряду С10 - С102 - - С103 - С1О4 - окислительно-восстановительная активность ионов снижается. [14]
Из уравнений видно, что концентрация Н особенно сильно влияет здесь на величину окислительно-восстановительного потенциала раствора, а следовательно, и на его окислительно-восстановительную активность. [15]
Страницы: 1 2