Третичная алкила
Cтраница 1
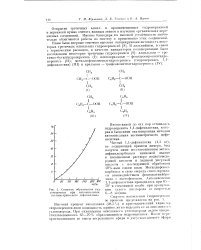 |
Скорость образования гидроперекиси при автоокислешш несимметрического дифепилэтана. [1] |
Открытие третичных алкил - и арилзамещенных гидроперекисей и перекисей нужно считать важным этапом в изучении органических нсре-кисных соединений. Именно благодаря их высокой устойчивости значительно облегчаются работы по синтезу и применению этих соединений. [2]
Обнаружено, что димерную структуру имеют также третичные алкилы и третичные арилы алюминия, такие как триметил ( 14), триэтил и трифенил. Но так как в этих структурах связь носит электронно-дефицитный характер ( мости-ковый атом углерода образует более, чем четыре связи), ее обсуждение мы отложим до гл. [3]
Если одновременно с метильными или метиленовыми группами присутствуют ароматические радикалы или третичные алкилы, то окисляются метальные или метиленовые группы. [4]
Окисление в присутствии кобальтового хелата первичных и вторичных ал-килов в бензольном ядре приводит к образованию карбонильных групп, не затрагивая третичные алкилы; получаются третичные ал-килзамещенные карбоновые кислоты, которые используются при производстве каучука. [5]
Вероятно, не существует принципиальных ограничений со стороны структуры гидроперекиси для ее успешного использования в качестве окислителя. Во многих патентах высказываются предположения, по-видимому достаточно обоснованные, о возможности применения в процессах эпоксидирования вторичных и третичных алкил - и циклоалкилгидроперекисей, гидроперокси-олефинов и аралкилгидроперекисей. Считается также возможным использование кетогидроперекисей, гидропероксиэфиров и фе-нольных гидроперекисей. Однако тщательный просмотр оригинальной и патентной литературы позволяет убедиться в том, что список гидроперекисей, фактически используемых для окисления олефинов различного строения, не так уж и велик. [6]
При этом алкиновые реагенты наименее реакционносггособггы, но обеспечивают наибольшую подвижность других групп R. Наиболее активными реагентами являются соединения, у которых Х - трет-бутил. Та же реакция соединений, содержащих вторичные или третичные алкилы, протекает с одинаковым выходом продуктов алкплирования по обоим углеродным атомам, связанным тройной связью. [7]
Выбор восстановителя зависит обычно от того, какие другие функциональные группы присутствуют в молекуле. Каждый из реагентов одни группы восстанавливает, а другие - нет. В-н-бу - тил-9 - ББН [883] ( реакция 10 - 101) восстанавливают третичные алкил -, бензил - и аллилгалогениды, но не реагируют с первичными или вторичными алкил - и арилгалогенидами. [8]
Реакция находит широкое применение и может быть проведена для субстратов, содержащих различные функциональные группы. Для связывания образующегося НХ часто добавляют основание. В методе Шот-тена - Баумана используется водный раствор щелочи, но часто применяется пиридин. Как R, так и R могут быть первичными, вторичными или третичными алкилами или арилами. По этой же методике можно приготовить сложные эфиры енолов, хотя при этом возникает конкуренция с С-алкилированием. [9]
Страницы: 1