Циклопропановое кольцо
Cтраница 2
Поскольку образование циклопропанового кольца происходит через енольную форму исходного соединения, такие процессы называются еноленовымн перегруппировками или гомо - [1,5] - сигматропным сдвигом водорода. [16]
Своеобразные свойства циклопропанового кольца, как уже упоминалось, связывают с особым состоянием гибридизации составляющих его углеродных атомов, с наличием банановых связей в циклопропане. Эти же причины оказывают определенное влияние и на стереохимию реакций замещения в циклопропане. [17]
Изучение раскрытия циклопропанового кольца в 1-аршщиклопропано-лах при нагревании ( 50 С) с 0OilN спиртовым раствором едкого натра показало, что в этом случае ( в противоположность кислотному раскрытию) заместители в ариле почти не влияют на скорость реакции. Это свидетельствует о том, что в щелочах раскрытие проходит в сторону наиболее устойчи-зого карбаниона. [18]
Степень участия удаленного циклопропанового кольца существенно зависит от его относительной ориентации. [19]
Изменение ориентации циклопропанового кольца относительно бисек-торной плоскости от 0 до 90 в ряду конформационно жестких га-нитрофенил-циклопропанов мало меняет электронное взаимодействие между циклопро-пильной группой и нитрофенильным или фенильным хромофором, что следует из изучения электронных спектров таких соединений. [20]
Присутствие в циклопропановом кольце алкоксильного заместителя способствует еще более легкому протеканию реакции. [21]
Таким образом, циклопропановое кольцо более эффективно передает электронное влияние заместителей. [22]
Таким образом, циклопропановое кольцо в этой реакции действительно проявляет свойство я-системы. [23]
Реакция протекает через протонированное циклопропановое кольцо. [24]
При введении в циклопропановое кольцо электроноакцепторных групп химический сдвиг метиленовых и метиновых протонов кольца понижается. В результате становится возможным наложение сигналов не только метиновых, но и метиленовых протонов циклопропанового кольца на сигна-лн алифатических протонов алкильных заместителей. [25]
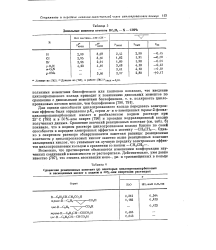 |
Днпольные моменты кетонов RCeH4 - X - COPh. [26] |
Для оценки способности циклопропанового кольца передавать электронные эффекты были определены рКа серии м - и и-замещенных пграис-2 - фенил-циклопропанкарбоновых кислот в разбавленном водном растворе при 25 С [795] и в 50 % - ном спирте [796] и проведен корреляционный анализ полученных данных. [27]
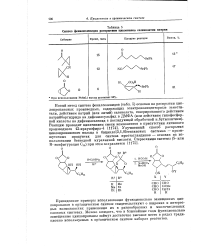 |
Синтез фенилселенидов раскрытием циклонанов селенолатом натрия. [28] |
Улучшенный способ раскрытия циклопропанового кольца в бицикло [3,1,0] гексановых системах - промежуточных продуктах для синтеза простагландинов - основан на использовании безводной муравьиной кислоты. [29]
Альдегидная группа при циклопропановом кольце окисляется без раскрытия циклопропанового кольца в карбоксильную. [30]
Страницы: 1 2 3 4