Комплекс - кальций
Cтраница 1
Комплексы кальция с полиаминополиуксусными кислотами ( комплексонами) имеют важное значение для аналитической химии кальция. На применении их основаны титриметрические методы определения кальция. [1]
Комплексы кальция обычно координационно ненасыщенны и образуют в водной среде устойчивые гидраты. Последние могут экстрагироваться органическими растворителями только при замене координационной воды полярным органическим растворителем. [2]
Комплекс кальция с мурексидом относительно малоустойчив и переход окраски недостаточно резкий и ясный. Титрование ведут в присутствии перетитрованной пробы. [3]
Комплексы кальция обычно координационно ненасыщенны и образуют в водной среде устойчивые гидраты. Последние могут экстрагироваться органическими растворителями только при замене координационной воды полярным органическим растворителем. [4]
Комплексы кальция с полиаминополиуксусными ки слотами ( комплексонами) имеют важное значение для аналитической химии кальция. На применении их основаны титриметрические методы определения кальция. [5]
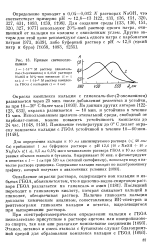 |
Кривые светопогло -., щения. [6] |
Окраска комплекса кальция с глиоксаль-бггс - ( 2-оксианилом) развивается через 25 мин. По данным других авторов [122-123, 633], окраска развивается - 10 мин. [7]
Гексаква - комплекс кальция [ Са ( Н2О) в ] 2 под действием магнитного поля может заполнять эти структуры, обусловливая их стабильность. То же может происходить и с растворенными в воде газами, вследствие чего их концентрация снижается. [8]
 |
Кривые спектрофотометрического комплексометрического титрования кальция в присутствии мурексида ( а и меди ( II в аммиачной среде ( б. [9] |
В точке эквивалентности, когда комплекс кальция с мурексидом разрушается и образуется комплекс кальция с ЭДТА, наблюдается резкое уменьшение светопоглощения. За точкой эквивалентности поглощение снова остается постоянным. Титрант вблизи точки эквивалентности следует добавлять небольшими порциями, чтобы точно зафиксировать резкое изменение светопоглощения. [10]
В фильтрате после отделения магния комплекс кальция с тр илоном Б разрушают кипячением с перекисью водорода потому, что он образует с кальцием в щелочной среде более прочный комплекс, чем арсеназо. [11]
Определение состава и константы нестойкости щавелевокислого комплекса кальция проводят статическим методом ионного обмена при комнатной температуре. [12]
В присутствии ионов кальция могут образоваться комплексы кальция с протеинами, которые могут адсорбироваться на поверхностях и сохраняться. Образующиеся же при расщеплении белков аминокислоты хотя и растворимы в воде, но вряд ли вымываются из донного ила при отсутствии движения воды и, вероятно, служат базой для биосинтеза. [13]
Метод, основанный на измерении светопоглощения комплекса кальция с комплексоном III при 225 нм, рекомендован для быстрых определений, когда не требуется высокая точность. [14]
В данной работе необходимо определить состав и константу нестойкости щавелевокислого комплекса кальция. [15]
Страницы: 1 2 3 4