Комплекс - двухвалентный кобальт
Cтраница 1
Комплексы двухвалентного кобальта ( 2: 1) могут превращаться в указанные выше комплексы при обработке минеральной кислотой в присутствии кислорода воздуха, и это, без сомнения, объясняет противоречивость результатов, полученных предыдущими исследователями. [1]
Очевидно, комплексы двухвалентного кобальта с координа-юнным числом 6 должны иметь моменты, Соответствующие ному непарному электрону, при условии, что связи ковалентны; ггаэдрические комплексы с трехвалентным кобальтом должны 1ть диамагнитными. Исключениями являются, вероятно, гексафторид и не-торые нитрозокомплексы, о которых мы скажем несколько зже. [2]
Сведения о комплексах двухвалентного кобальта триаминово-го типа малочисленны. Комплексы с тиомочевиной окрашены в розовый цвет, что рассматривается некоторыми авторами как доказательство тетраэдрического строения. Более достоверных сведений о строении этих соединений пока не получено. [3]
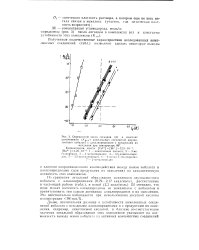 |
Определение числа лигандов ( п н констант устойчивости ( Куст комплексных соединений двухвалентного кобальта с алкилпиридииами и продуктами их. [4] |
Из сравнения энтальпий образования комплексов двухвалентного кобальта с алкилпиридииами ( 0 79 - 2 17 ккал / моль), рассчитанных в настоящей работе ( табл.), и водой ( 2 3 ккал / моль) [5] очевидно, что вода может вытеснять алкилпиридины из комплексов с кобальтом и препятствовать тем самым активации алкилпиридинов и их окислению. Это действительно наблюдается при использовании уксусной кислоты концентрации 98 мас. [5]
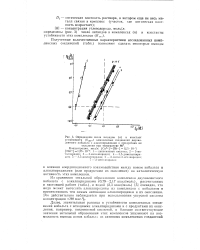 |
Определение числа лигандов ( п и констант устойчивости ( Куст комплексных соединений двухвалентного кобальта с алкнлпиридипами и продуктами их. [6] |
Из сравнения энтальпий образования комплексов двухвалентного кобальта с алкилпиридинами ( 0 79 - 2 17 ккал / моль), рассчитанных Б настоящей работе ( табл.), и водой ( 2 3 ккал / моль) [5] очевидно, что вода может вытеснять алкилпиридины из комплексов с кобальтом и препятствовать тем самым активации алкилпиридинов и их окислению. Это действительно наблюдается при использовании уксусной кислоты концентрации О8 мас. [7]
Повндимому, это означает неустойчивость комплексов двухвалентного кобальта с шестерной координацией. Аналогично, в гипотетических ионах Ni ( CN) 5 - n Ni ( CN) 6 - нужно было бы поместить в оболочку 4d один и два электрона соответственно. [8]
 |
Строение комплекса в соединении [ Co ( NH3 5 ( N3 ] ( N3. [9] |
Расстояния Со - С1 имеют значения 2 26 - 2 27 А; они значительно короче, чем в октаэдрических ( но высокоспиновых) комплексах двухвалентного кобальта. [10]
Джекобсон [6] - аналогичный распад под влиянием комплексов двухвалентного кобальта. Джонассен [10] показал, что комплекс двухвалентного кобальта с трис - ( 2-аминоэтил) амином катализирует разложение перекиси водорода. [11]
В этом случае ЭСКП еще довольно мала и вряд ли будет решающим фактором в определении строения комплексов элементов первого переходного периода. До сих пор свойства комплексов d2 как следует не изучены, но хорошо известно, что многие комплексы двухвалентного кобальта конфигурация) являются тетра-эдрическими. [12]
Дру [25] предложил для медного, никелевого и кобальтового комплексов фенилазо-р-нафтиламйна - структуры ( XXIX), аналогичные структуре ( XXV) соответствующих комплексов фенилазо-р-нафтола. Однако недавно появилась работа [34], в которой на этот счет высказано сомнение, так как в отличие от комплексов двухвалентного кобальта фенилазо-р-нафтола ( 2: 1), имеющих тет-раэдрическую структуру, ( 2: 1) комплексы Со11 фенилазо-р-наф-тиламина обладают плоским строением. [13]
Джекобсон [6] - аналогичный распад под влиянием комплексов двухвалентного кобальта. Джонассен [10] показал, что комплекс двухвалентного кобальта с трис - ( 2-аминоэтил) амином катализирует разложение перекиси водорода. [14]
Некоторые из этих комплексов существу ] в двух видах, отличающихся иногда весьма сильно по восприимч вости. Магнитные измерения показывают, что у двухвалентно кобальта имеется тенденция к образованию преобладающе ио ных октаэдрических и тетраэдрических комплексов, если свя с группами осуществляются через атомы азота, кислорода и. Для примера в табл. 30 показаны к которые комплексы двухвалентного кобальта и их магнитш моменты. [15]
Страницы: 1 2