Комплекс - литий
Cтраница 1
Комплексы лития, натрия и калия с этими двумя лигандами хроматографировались отдельно и в смеси на колонке длиной 90 см с носителем, покрытым 2 5 % силиконовой смолы Е-301, при 200 С, при пропускании тока азота. [1]
Комплекс лития с дибромоксихинолином образуется в щелочном этанольном растворе, который флуоресцирует зеленым цветом. В спектре поглощения комплекса дибром-оксихинолината лития наблюдается два максимума при 345 и 385 нм. Наименьшее обнаруживаемое количество лития в этанольном растворе 0 1 мкг / мл Li. Реакции не мешают до 1 5 мг других щелочных металлов. [2]
Интенсивные исследования в области купратных комплексов лития, проводимые в настоящее время, расширяют синтетические возможности литийорганических соединений, из которых они легко получаются. [3]
Известные по литературным данным реакции образования комплексов лития с органическими реагентами протекают в сильнощелочной среде. Часть из них, а именно реакции образования скрашенных соединений, используемые для качественного определения лития в водной и водно-ацетоновой средах, были рассмотрены в гл. Здесь же будут описаны реакции комплексо-образования, на основании которых разработаны экстракционные методы отделения лития. [4]
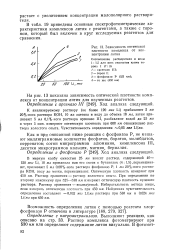 |
Зависимость оптической плотности комплекса от концентрации лития. [5] |
В табл. 19 приведены основные спектрофотометрические характеристики комплексов лития с реагентами, а также с торо-ном, который был включен в круг исследуемых реагентов для сравнения. [6]
К числу чувствительных реакций на литий относятся реакции, основанные на образовании комплексов лития с рядом реагентов, флуоресцирующих при облучении УФ-светом. Одной из давно известных является реакция лития с 8-оксихинолином. [7]
Комплекс 5 7-дибром - 8-оксихинолина с ионом лития флуоресцирует более интенсивно, чем комплекс лития с 8-оксихинолином. На рис. 16 приведены спектры поглощения и флуоресценции комплекса лития с 5 7-дибром - 8-оксихинолином в среде этанола. [8]
 |
Скорость превращения при Ш С [ 7SJ. [9] |
Активность зависит также от размеров атомов щелочного металла: самая низкая активность у комплексов лития, а самая высокая у комплексов цезия. При хемосорбцни водорода окраска комплекса исчезает вследствие образования дигидроаниона, который взаимодействует с непредельным соединением и гидрирует его. [10]
В полярных средах в качестве инициаторов широко применяются также металлоароматические комплексы, в том числе комплексы лития, получающиеся при взаимодействии щелочных металлов с полиядерными ароматическими соединениями в среде ТГФ и ДМЭ. [11]
Позже аналогичные комплексы были найдены и для многих других элементов, не обладающих электронами на недостроенных внутренних оболочках ( например, комплексы лития и натрия), вследствие чего можно сказать, что изучение комплексов р.з.э. сыграло особую роль в общей химии комплексных соединений. [12]
Позже аналогичные комплексы были найдены и для многих других элементов, не обладающих электронами на недостроенных внутренних оболочках ( например, комплексы лития и натрия), вследствие чего можно сказать, что изучение комплексов р.з.э. сыграло особую роль в общей химии комплексных соединений. [13]
Комплекс лития с тороном нерастворим в хлороформе, бу-таноле и амилацетате. [14]
Комплекс 5 7-дибром - 8-оксихинолина с ионом лития флуоресцирует более интенсивно, чем комплекс лития с 8-оксихинолином. На рис. 16 приведены спектры поглощения и флуоресценции комплекса лития с 5 7-дибром - 8-оксихинолином в среде этанола. [15]
Страницы: 1 2