Комплекс - медь
Cтраница 2
Комплексы меди, одновалентные и двухвалентные, в сочетании с Cl -, Bi -, S0g - и NH3 лабильны. [16]
Циклооцтиновые комплексы меди ( C8H12) CuBr, ( C8H12) 2CuBr и золота ( C8H12) 2AuBr поглощают при 2060, 2085 и 2035 см 1 соответственно ( ср. [17]
Нерастворимый, незаряженный комплекс меди с а-бензоинок-симом ( купроном) состава 1: 1, возможное строение которого показано формулами XCI и XCII, обязан своей малой растворимостью большому числу фенильных групп, приходящихся на одну группу, способную координировать молекулы воды. С другой стороны, если анионный кислород способен служить донором электронов для второго атома меди, возможно образование трехмерной макромолекулы. Реагент отличается хорошей избирательностью по отношению к меди, но в кислых средах образует также осадки ( неизвестного строения) с молибдатами, вольфраматами, ванадатами и солями уранила. [18]
Известны комплексы меди ( 1) как с лигандами, не образующими я-связей, так и с лигандами рл - и cfat - типа, например с олефинами и ацетиленами. [19]
 |
Константы нестойкости некоторых комплексов при 25 С. [20] |
Однако комплекс меди быстро реагирует с сильной кислотой, в то время как комплекс кобальта не обнаруживает видимых изменений в ее растворе. Дело в том, что комплекс меди лабилен, а комплекс кобальта инертен и скорость его реакции с кислотой чрезвычайно мала. Ситуация с комплексом кобальта аналогична уже известной нам для смеси водорода с кислородом при комнатной температуре. Такая смесь также термодинамически неустойчива, но из-за высокого барьера активации реакция протекает с пренебрежимо малой скоростью. [21]
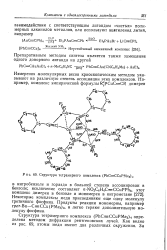 |
Структура тетрамерного комплекса ( PhCCCuPMe3 4. [22] |
Некоторые комплексы меди присоединяют еще одну молекулу третичного фосфина. Продукты реакции мономерны, например трет - Ви-С ССи ( РМе3) 2, и легко теряют дополнительную молекулу фосфина. [23]
Избытком комплекса меди ( Н) с амином осаждают [ Cu ( Big) 2 ] X2, после чего определяют избыток меди ( П) в растворе потенциомет-рическим титрованием с индикаторным Си2 - селективным электродом. [24]
Для изоструктурного комплекса меди также установлена плоская квадратная координация атома металла. Это противоречит утверждению Холла, Уотерса и др. [95, 140, 141, 145] о том, что в комплексах меди с зеленой окраской координационное число атома металла выше четырех. [25]
Обработка ацетонитрильным комплексом меди ( 1) [116] приводит к количественной реставрации гемоцианина [105, 117], на что указывает восстановление его полос поглощения, обусловленных медью, и его способности обратимо связывать кислород. Интенсивность полос меди при последовательном увеличении ее содержания в частично реставрированном холоферменте возрастает в квадратичной зависимости от количества связанной меди. [26]
В комплексах меди дополнительные лиганды находятся на большом расстоянии от центрального атома тю сравнению с плоскостными лигандами; в данном случае говорят об октаэдрическом ( 4 2) расположении лигандов. Однако существует ряд квазиплоских хелатов Си2 только с одним дополнительным лигандом. В этом комллексе Си2 имеет координационное число пять [ ( 4 1) - координация ], и центральный атом выступает над плоскостью цикла бис - ( глиоксиматодифенилбора) в направлении пятого лиганда. Кобальт ( П) имеет один неспаренный электрон как в плоских квадратных, так и в октаэдрических комплексах. Но, поскольку в октаэдрических комплексах он расположен на более высоком энергетическом уровне, октаэдрлческая структура встречается чаще. Тип структуры очень сильно зависит от природы лиганда. В плоских квадратных комплексах Fe2 и Мп2 имеют два и три неспаренных электрона соответственно, а в октаэдрических - ни одного или один. И действительно, эти металлы очень редко образуют плоские структуры. [27]
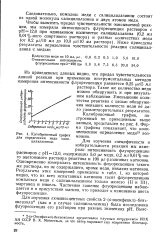 |
Калибровочный график для определения меди салицилалазином. [28] |
Следовательно, комплекс меди с салицилалазином состоит из одной молекулы салицилалазина и двух атомов меди. [29]
Куприэнат ( комплекс меди с этилендиамино м - [ Си - еп2 ] 2) образует с анионным комплексом [ CdJJ2 - труднорастворимое соединение, выделяющееся в виде крупных кристаллов. Для выполнения реакции к раствору соли кадмия прибавляют избыток KJ и затем куприэнат [ 42, стр. [30]
Страницы: 1 2 3 4