Окрашенный комплекс - металл
Cтраница 1
Окрашенные комплексы металлов образуются только в тех случаях, когда в молекуле органического реагента имеются хромофорные группы с я-электронами; циклическая группа также может входить в я-электронную систему, однако между ацы-группой и системой сопряженных связей молекулы не допускается ни одной изолирующей группы ( см. разд. Если конфигурация молекулы допускает-образование плоского комплекса, то в результате делокализации электронов может наблюдаться батохромный сдвиг. [1]
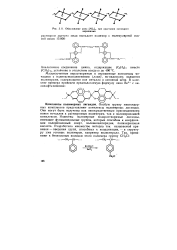 |
Образование иона [ MLs ]. при срастании октаз дров вершинами. [2] |
Малоизученные нерастворимые и окрашенные комплексы металлов с полиоксисоединениями ( лаки), по-видимому, являются полимерами, содержащими ион металла в основной цепи. [3]
Образование окрашенных комплексов металлов с органическими реагентами широко используют в качественном и количественном неорганическом и органическом анализе. Для определения металлов чаще всего используют комплексо-образующие реагенты. [4]
Сущность указанного метода исследования состоит в применении окрашенных комплексов металлов, которые обесцвечиваются при добавлении аддендов вследствие образования бесцветных комплексов металла с аддендом. Роль окрашивающего компонента заключается лишь в том, чтобы сделать видимым один из компонентов равновесия, что дает возможность определять различные изменения в системе, обусловленные комплексообразованием. [5]
Таким образом, характер взаимодействия во многом аналогичен образованию других окрашенных комплексов металлов со слабыми кислотами. [6]
Ниже в табл. 11 приведены данные [15-22] о некоторых окрашенных комплексах металлов с перекисью водорода, которые имеют значение для фотометрического анализа; менее достоверные данные даны в скобках. [7]
Все методы фотометрического определения фторидов основаны на реакции ионов фтора с окрашенными комплексами металлов. При этом обычно предполагается конкурирующая схема ( 3); ионы фтора связывают металл во фторидный комплекс, вследствие чего уменьшается концентрация окрашенного комплекса. Ослабление оптической плотности приблизительно соответствует расчетам. Однако и в этих случаях часто вместо простого понижения полосы поглощения окрашенного комплекса наблюдается также сдвиг волны максимума. [8]
Кроме того, исследования сольватохромии относятся к органическим красителям, а не к окрашенным комплексам металлов. [9]
Большинство методов определения фтористого водорода и фторидов основано на взаимодействии иона фтора с окрашенными комплексами металлов, в результате чего происходит постепенное ослабление или изменение первоначальной окраски раствора. [10]
При повышении же рН окрашенные комплексы ( соли слабых кислот) часто становятся настолько прочными, что не реагируют с ионами фтора: малопрочные окрашенные комплексы металлов, например роданид железа, при повышении рН разрушаются. [11]
Очевидно, концентрация ионов водорода при колориметрических определениях играет очень важную роль, и при использовании колориметрических методик надо руководствоваться следующими положениями: реакции образования окрашенных комплексов металлов с анионами сильных кислот следует проводить в кислых средах; если реактив является слабой кислотой, то с повышением рН степень связывания иона металла в комплекс возрастает. Однако при повышении рН раствора надо учитывать ступенчатость комплексообразования, проявление индикаторных свойств реактивом и возможность образования окрашенных комплексов реактивом с посторонними ионами; интервалы рН, при которых следует проводить реакцию, как правило, определяют экспериментально. При проведении анализа химик должен строго придерживаться прописи, указанной в методике. [12]
Можно назвать далее интересные работы по применению некоторых металлохромных индикаторов, которые вначале были рекомендованы в качестве индикаторов при комплексонометрическом титровании. Окрашенные комплексы металлов с некоторыми металлохром-ными индикаторами способны экстрагироваться. [13]
При колориметрических методах большое значение для точности определения имеет рН растворов. Окрашенные комплексы металлов с анионами сильных кислот ( SCN -, Cl -, J -) обычно образуются в кислых растворах. Анионы сильных кислот не связываются с ионом водорода в молекулу кислоты, поэтому повышение кислотности в довольно широких пределах не вызывает какого-либо нарушения равновесия образования окрашенного комплекса. Наоборот, заметное уменьшение кислотности ( повышение рН) обычно недопустимо. Поэтому при увеличении рН раствора такие окрашенные соединения разлагаются с образованием осадка гидроокиси металла или основной соли. [14]
При колориметрических методах большое значение для точности определения имеет рН растворов. Окрашенные комплексы металлов с анионами сильных кислот ( SCN -, Cl -, 1 -), обычно образуются в кислых растворах. Анионы сильных кислот не связываются с ионом водорода в молекулу кислоты, поэтому повышение кислотности в довольно широких пределах не вызывает какого-либо нарушения равновесия образования окрашенного комплекса. Наоборот, заметное уменьшение кислотности ( повышение рН) обычно недопустимо. Поэтому при увеличении рН раствора такие окрашенные соединения разлагаются с образованием осадка гидроокиси металла или основной соли. [15]
Страницы: 1 2