Комплексо-нат
Cтраница 2
Обратным титрованием пользуются, когда нельзя подобрать индикатор или подходящую физическую величину для нахождения скачка кривой при прямом титровании, когда комплексо-наты образуются медленно и когда при рН раствора, необходимого для осуществления прямого титрования, определяемые ионы металла образуют осадок соответствующего гидроксида или основной соли. [16]
Сочетание таких свойств, как: 1) комплексование всех присутствующих IB водных растворах катионов; 2) термическое разложение комплектна и комплексо-натов при температурах 280 - 300 С с образованием магнетита иа поверхности металла при термолизе комплектна тав железа, делает аммонийную соль ЭДТК в настоящее время единственно возможным реагентом для принудительного высаживания соединений железа в менее тешюнапряжеяных поверхностях йагрева. [17]
Метод основан на осаждении фтор-иона титрованным раствором СаСЬ, избыток которого титруется трилоном Б с хромоген черным, в присутствии небольшого количества комплексо-ната магния. [18]
Для измерения выбирают спектральную область, соответствующую Ямакс 265 нм, в которой определяемое вещество ( комплексо-нат висмута) поглощает излучение, а второе вещество ( комплексо-нат свинца) его не поглощает. [19]
Сущность метода заключается в том, что ионы Са2 в щелочной среде образуют комплексное соединение с индикатором мурекси-дом, которое разрушается при титровании трилоном Б в результате образования более устойчивого комплексо-ната кальция. [20]
Как видно из приведенных уравнений, независимо от заряда катиона, реакция комплексообразования всегда протекает в соотношении 1 атом металла на 1 моль трилона Б, причем освобождается 2 эквивалента водорода. Образующиеся комплексо-наты различаются лишь по числу своих отрицательных зарядов. [21]
Этот комплекс разрушается комплексоном III с изменением окраски раствора из винно-красной в синюю. Вследствие малой прочности комплексо-ната магния реакция между магнием и комплексоном III протекает не мгновенно. Нест комплексов магния с комплексоном III и эриохром черным Т окраска раствора в эквивалентной точке меняется не очень резко. [22]
Однако следует заметить, что прочность комплексов возрастает не пропорционально уменьшению расстояния между атомами азота в молекуле лиганда. Последовательность изменения констант устойчивости комплексо-натов имеет следующий порядок: ттгранс - ЦГДТА торанс - ЦПДТА uc - ЦГДТА, - тогда как расстояние между атомами азота ком-плексообразующих групп - N ( CH2COOH) 2 уменьшается в другой последовательности: г / ис - ЦГДТА 5 траис - ЦГДТА транс - ЦПДТА. Пониженная устойчивость хелатов щелочноземельных металлов с мс - ЦГДТА вызвана стереохимическими помехами при реакции хелатообразования. [23]
Для определения сульфат-ионов их осаждают в виде сульфата бария. Осадок потом растворяют в аммиачном растворе комплексо-ната III и анализ завершают титрованием избытка комплексона III раствором ионов магния. [24]
Сг ( VI) осаждается неполностью в виде оксихинолината; до 20 мг Сг ( VI) мешает очень мало. Кроме того, хром можно связать в комплексо-нат кипячением с комплексоном III в течение 5 мин. Титан полностью осаждается в виде оксихинолината при рН 9 и ниже, при рН 9 осаждение неполное. [25]
При этом освобождаются два грамм-иона водорода. Для того чтобы обеспечить значение рН среды, необходимое для образования комплексо-ната, применяют буферный раствор. [26]
Кальций в металлическом натрии определяют объемным комплексонометрическим методом. Для более четкого перехода окраски в точке эквивалентности определение проводят в присутствии комплексо-ната магния. [27]
Однако даже и в тех случаях, когда стехиометрия реакции изменяется при изменении рН, как, например, при взаимодействии ЭДТА с Fe111, когда при рН 1 5 - 4 образуется нормальный комплексонат FeY - ( lgP 25 l) прирН5 - 6 - гидроксокомплексонат Fe ( OH) Y2 - ( lgp 7 5), при рН 6 - 9-аналогичный комплекс с двумя ионами гид-роксила Fe ( OH) 2Y3 ( lgp 9 4), титрование возможно. Образование двух последних комплексов нежелательно, так как они существенно отличаются от нормального комплексо-ната по устойчивости. Это препятствует удовлетворительному протеканию аналитической реакции комплексообразования. [28]
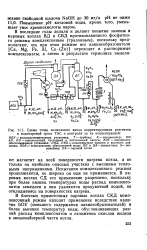 |
Схема точек возможного ввода корректирующих реагентов в водопаровой тракт ТЭС и контроля за их концентрацией. [29] |
Испытания комплексонного режима продолжаются, но широко он еще не применяется. В паровых котлах СД его применение разрешено, поскольку при более низких температурах воды распад комплексо-натов замедлен и они удаляются продувочной водой, не откладываясь на поверхностях нагрева. [30]
Страницы: 1 2 3