Рассматриваемый комплексон
Cтраница 1
 |
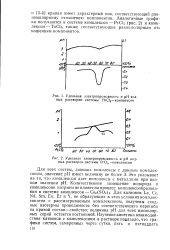
Кривые нейтрализации полиметилендн-аминтетрауксусных кислот ( для 1 - 4 и Г-4 величина п изменяется соответственно от 2 до 5. [1] |
Рассматриваемые комплексоны обладают высокой скоростью комплексообразования и отличаются значительно лучшей растворимостью в воде, чем ЭДТА, что весьма важно для практического применения. Специфика хелатообразования этих комплексонов вызвана, вероятно, ограничением вращения отдельных частей молекулы относительно этиленового мостика в результате введения ме-тильных групп, что способствует стабилизации комплекса. [2]
Анализ величин констант диссоциации рассматриваемых комплексонов ( табл. 45) дает основание сделать вывод о бетаиновом строении этих соединений и о механизме депротониза-ции их. [3]
 |
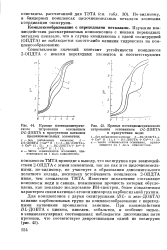
Удельная электропроводность и рН водных растворов системы YbCl3 - комплексом.| Удельная электропроводность и рН водных растворов системы РгС13 - комплексов. [4] |
Для катионов La, Се, Nd, Sm, Eu, Er и Y, не образующих в этих условиях комплек-сонатов с рассматриваемым комплексоном, получены сходные изотермы проводимости без соответствующего перегиба на кривой состав-свойство; величина рН для всех изомоляр-ных серий остается постоянной. [5]
 |
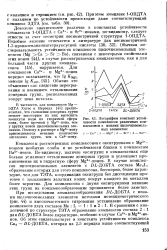
Кривые потенциометриче.| Кривые потенциометрического титрования основанием.. - ДОБТА. [6] |
Изучение взаимодействия рассматриваемых комплексонов с ионами переходных металлов показало, что в случае комплексона с одной оксигруппой ( ОПДТА) не наблюдается какого-либо влияния гидроксила на ком-плексообразование. [7]
 |
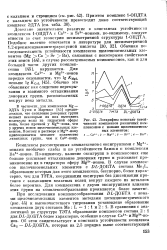
Логарифмы констант устойчивости комплексов различных комплексонов с ионами щелочноземельных элементов. [8] |
Довольно значительное различие в константах устойчивости комплексов 1 - ОПДТА с Са2 - и Sr2 - ионами, по-видимому, следует отнести за счет геометрии несимметричной структуры 1 - ОПДТА. Обычная последовательность устойчивости комплексов щелочноземельных элементов ( Mg Ca Sr Ba), связанная с некоторыми свойствами этих ионов [44], в случае рассматриваемых комплексонов, как и для большей части других комплексонов [45], нарушается. Обычно это объясняют как следствие перекрывания и взаимного отталкивания донорных групп, расположенных вокруг иона металла. [9]
 |
Логарифмы констант устойчивости комплексов различных комплексонов с ионами щелочноземельных элементов. [10] |
Довольно значительное различие в константах устойчивости комплексов 1 - ОПДТА с Са2 - и Sr2 - ионами, по-видимому, следует отнести за счет геометрии несимметричной структуры 1 - ОПДТА. Обычная последовательность устойчивости комплексов щелочноземельных элементов ( Mg Ca Sr - Ва), связанная с некоторыми свойствами этих ионов [44], в случае рассматриваемых комплексонов, как и для большей части других комплексонов [45], нарушается. Обычно это объясняют как следствие перекрывания и взаимного отталкивания донорных групп, расположенных вокруг иона металла. [11]
Увеличение дентатности комплексона в результате введения дополнительных фосфоновых групп вызывает увеличение прочности образуемых комплексов. Так, этилендиаминтетраметилфосфоновая и диэтилентриаминпентаметилфосфоновая кислоты являются более сильными комплексообразующими агентами по отношению к редкоземельным элементам, чем карбоксилсодержащие аналоги. Устойчивость нормальных комплексов рассматриваемых комплексонов намного выше устойчивости соответствующих комплексов этиленди-аминтетрауксусной кислоты и не уступает устойчивости комплексов диэтилентриаминпентауксусной кислоты, считающейся оптимальным реагентом при комплексообразовании с редкоземельными элементами. Комплексы редкоземельных элементов с ЭДУФ по устойчивости также превышают комплексы с ЭДТА, исключение составляют лишь комплексы лютеция и иттербия. [12]
Увеличение дентатности комплексона в результате введения дополнительных фосфоновых групп вызывает увеличение прочности образуемых комплексов. Так, этилендиаминтетраметилфосфоновая и диэтилентриаминпентаметилфосфоновая кислоты являются более сильными комплексообразующими агентами по отношению к редкоземельным элементам, чем карбоксилсодержащие аналоги. Устойчивость нормальных комплексов рассматриваемых комплексонов намного выше устойчивости соответствующих комплексов этиленди-аминтетрауксусной кислоты и не уступает устойчивости комплексов диэтилентриаминпентауксусной кислоты, считающейся оптимальным реагентом при комплексообразовании с редкоземельными элементами. Комплексы редкоземельных элементов с ЭДУФ по устойчивости также превышают комплексы с ЭДТА, исключение составляют лишь комплексы лютеция и иттербия. [13]
Страницы: 1