Комплексооб-разователь
Cтраница 2
Практически все элементы могут играть роль комплексооб-разователя. Однако наибольшее число комплексных соединений известно для d - элементов 4 -, 5 - и 6-го периодов системы. В качестве примера того, что и элементы 2-го периода способны быть комплексообразователем ( лишь бы они могли стать акцепторами пар электронов), можно рассмотреть образование комплексного соединения лития. Атом лития имеет электронную конфигурацию Is22sl2p и при образовании иона Li теряет один электрон. [16]
Центральный ион или атом комплекса называют комплексооб-разователем. [17]
Та особенность, что координационное число большинства комплексооб-разователей равно 6, а многих других равно 4, находит свое объяснение в пространственном расположении групп. Предполагают, что у веществ с координационным числом 6 центральный ион находится в серединэ правильного октаэдра, а 6 координационных связей его направлены к 6 углам октаэдра. У веществ с координационным числом 4 центральный атом предполагают находящимся в центре тетраэдра, а 4 координационные связи его направленными к 4 углам тетраэдра. Пользуясь таким допущением относительно пространственного строения комплексных солей, приходят к объяснению явлений структурной и зеркальной изомерии. Вещества одинакового химического состава, обнаруживающие, однако, различные физические свойства, называют изомерными. [18]
Применение осадителя при зонной плавке аналогично применению комплексооб-разователей в ионном обмене. При зонной кристаллизации нитрата аммония происходит встречное движение редкоземельных элементов и осадителя, тем самым создаются лучшие условия для избирательного осаждения. [19]
 |
Щелочные растворы для химического никелирования. [20] |
Между тем наличие в щелочных растворах таких комплексооб-разователей, как лимоннокислый натрий и аммиак, а также то обстоятельство, что в щелочной среде растворимость фосфитов значительно выше, чем в кислой, позволяло надеяться, что при регулярном корректировании щелочных растворов можно будет поддерживать максимальную скорость никелирования на постоянном уровне более длительное время, чем в кислых растворах. [21]
 |
Октаэдрическое поле лигандов. [22] |
При октаэдрическом расположении лигандов d - AO комплексооб-разователя попадают в неравноценное положение. Поэтому между электронами, заселяющими эти АО, и отрицательными зарядами лигандов возникают значительные силы отталкивания, приводящие к увеличению энергии dz2 - и dx2 - у2 - АО. Взаимодействие между dz2 -, dx2 - у2 - АО и близко расположенными к ним лигандами можно представить в виде сильно сжатой пружины. [23]
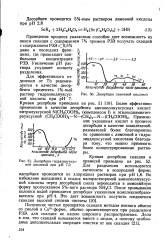 |
Десорбция лимонной кислотой.| Десорбция гидразинуксус-ной кислотой при рН 7 0. [24] |
Применение указанных кислот в процессе десорбции в качестве комплексооб-разователей более благоприятно по сравнению с лимонной и гидра-ть зиндиуксусной кислотами благодаря тому, что можно применять более концентрированные растворы. [25]
При экстракции металла органическим раствором комп-лексообразователя происходит распределение комплексооб-разователя, металла и комплекса. Рассмотрим все эти случаи. [26]
Элементы подгруппы галогенов в любых состояниях окисления являются слабовыраженными комплексооб-разователями. Однократно-отрицательные ионы галогенов по своей электронной структуре являются аналогами инертных газов и по своей способности к комплексообразованию примыкают к ним наряду с щелочными металлами. [27]
Из рассмотренного в основном тексте вытекает, что типичными комплексооб-разователями должны быть многозарядные ионы со сравнительно небольшим объемом. Так как элементарные анионы характеризуются небольшими заряда ми и значительными объемами, роль комплексообразо-вателя для них малохарактерна. Однако отдельные представители подобных комплексов все же известны, даже помимо аммонийных и оксониевых соединений. Из последних наиболее интересен основной ацетат бериллия ( XII § 1 доп. Значительно характернее для него координационное число 3, проявляющееся в ионе ОН3, комплексе [ O ( HgCl) 3 ] Cl ( XII § 4 доп. [28]
ТКП приложима лишь к комплексным соединениям, в которых комплексооб-разователь ( rf - элемент) имеет свободные электроны. Кроме того, детально разбирая изменения центрального атома, ТКП вовсе не учитывает ни структурных особенностей лигандов, ни склонности некоторых из них образовывать тг-связи. [29]
ТКП приложима лишь к комплексным соединениям, в которых комплексооб-разователь ( - элемент) имеет свободные электроны. Кроме того, детально разбирая изменения центрального атома, ТКП вовсе не учитывает ни структурных особенностей лигандов, ни склонности некоторых из них образовывать т-связи. [30]
Страницы: 1 2 3 4