Комплексообразо-вание
Cтраница 3
В последнем случае в процессе смешанного комплексообразо-вания происходит повышение к.ч. металла. [31]
Широко известна способность дипиридилов к комплексообразо-ванию с фенолами, аминами, солями металлов и другими соединениями. [32]
Последний имеет большую склонность к комплексообразо-ванию с некоторыми тяжелыми металлами. [33]
Тенденция галогена в алкилгалогенидах к комплексообразо-ванию с кислотами Льюиса обратно пропорциональна ионным объемам, поэтому устойчивость комплекса возрастает от ал-килиодида к алкилфторпду. Так, например, метилбромид в присутствии бромистого алюминия реагирует с бензолом примерно в 200 раз быстрее, чем йодистый метил. Поэтому для реакций алкилирования по Фриделю - Крафтсу алкилиодиды мало пригодны. [34]
Трехвалентный плутоний менее склонен к комплексообразо-ванию, чем четырехвалентный и шестивалентный. [35]
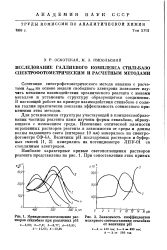 |
Кривые светопоглощения растворов стильбазо при различных рН.| Зависимость коэффициентов. [36] |
Для установления структуры участвующей в комплексообразо-вании частицы реагента нами изучены формы стильбазо, образующиеся с изменением среды. [37]
При значениях рН2 ионы водорода тормозят комплексообразо-вание, поэтому все ионы редкоземельных элементов находятся в растворе и монофункциональная иминодиуксусная смола в сильнокислой среде не проявляет емкость для этих ионов. [38]
В сложных случаях, когда происходит ступенчатое комплексообразо-вание металла с лигандом X, для вычисления константы скорости диссоциации kd необходимо пользоваться выражением в общем виде. При выводе этого выражения предполагалось, что реакцией, определяющей скорость процесса, является диссоциация комплекса МеХА на MeXft j и что электрохимически активными являются лишь свободный катион и комплексы от МеХ до MeXft-i, в то время как остальные комплексы от МеХ до МеХ считались неактивными. [39]
В сложных случаях, когда происходит ступенчатое комплексообразо-вание металла с лигандом X, для вычисления константы скорости диссоциации ka необходимо пользоваться выражением в общем виде. При выводе этого выражения предполагалось, что реакцией, определяющей скорость процесса, является диссоциация комплекса МеХй на MeX - i и что электрохимически активными являются лишь свободный катион и комплексы от МеХ до MeXft - b в то время как остальные комплексы от MeXft до МеХп считались неактивными. [40]
Еще более широко используется сам процесс комплексообразо-вания, протекающий с использованием как неорганических, так и органических реагентов, образующих с катионами комплексные и внутрикомплексные соединения. [41]
Данные, полученные для большинства реакций комплексообразо-вания, показывают, что хелатныи эффект вызван увеличением энтропии, но в ряде случаев он обусловлен и уменьшением энтальпии. [42]
Такое перераспределение свидетельствует о динамичности процесса комплексообразо-вания в зависимости от времени контактирования нефти с карбамидом. [44]
В случае, когда равновесие реакции комплексообразо-вания устанавливается медленно по сравнению с временем жизни капли или когда время установления равновесия сравнимо с временем жизни капли, на полярограм-мах наблюдают две волны. Первая волна, при более положительных потенциалах, соответствует восстановлению свободного иона. [45]
Страницы: 1 2 3 4