Комплексообразование
Cтраница 1
Комплексообразование, как правило, стабилизирует неустойчивую степень окисления. [1]
Комплексообразование, препятствуя передаче цепи при фотохимической или радиационной полимеризации сложных аллиловых эфиров, ускоряет реакцию и способствует образованию более высокомолекулярных продуктов. [2]
Комплексообразование на поверхности, как видно из изложенного, играет важную роль в формировании адгезионных связей. При получении композитов на основе неорганических клеев вклад адгезии в формирование физико-механических свойств материала существен. [3]
Комплексообразование происходит быстро и обратимо, а деметилиро-ванне - медленно н необратимо, поэтому через определенное время в реакционной смесн остаются только продукты деметнлнрования. При действии трнэтнламнна или карбонат-аниона протекает только деметнлнро-ванне, притом быстро. Подобная реакция деметилнрования известна и для соединений ннтроароматнческого ряда, но в данном случае она протекает особенно легко. [4]
Комплексообразование, как правило, стабилизирует неустойчивую степень окисления. [5]
Комплексообразование, препятствуя передаче цепи при фотохимической или радиационной полимеризации сложных аллиловых эфиров, ускоряет реакцию и способствует образованию более высокомолекулярных продуктов. [6]
Комплексообразование сопровождается снижением основности ПЭИ, а также вязкости водных растворов вследствие понижения гидрофильности при экранировании ионных группировок комп-лексообразующими ионами меди. Аммиакаты ПЭИ с медью и никелем могут быть полностью высушены. Полученные порошки в отличие от ПЭИ негигроскопичны. Следует отметить, что координационные соединения ПЭИ представляют собой поливалентные анионообменные смолы. [7]
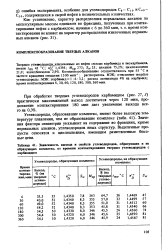 |
Зависимость выхода и свойств углеводородов, образующих и не образующих комплекс, от времени контактирования твердых углеводородов с карбамидом. [8] |
Комплексообразование осуществлялось при 55 С и частоте вращения мешалки 1500 мин 1; растворитель МЭК; отношение твердые углеводороды: МЭК: карбамид 1: 6: 3 2; расход активатора 4 % на карбамид; время контактирования 6, 30, 60, 120 180, 300, 360 мин. [9]
Комплексообразование с пикриновой кислотой используется как метод выделения полициклических ароматических углеводородов. Пикраты легко разлагаются горячей водой. Пикриновая кислота растворяется в воде, а полициклические ароматические углеводороды выделяются в свободном виде. [10]
Комплексообразование с кислотой Льюиса ведет к появлению частичного или целого положительного заряда на одном из атомов в молекуле хлора. [11]
Комплексообразование используют, кроме того, для так называемой маскировки ионов. [12]
Комплексообразование используют и для разделения металлов на анионитах. [13]
Комплексообразование наиб, характерно для переходных металлов. Из неметаллов центральным атомом служат чаще всего В, Р, Si, As. Лиганды представляют собой обычно анионы, напр. ОН - ( см. Гидроксокомплексы), остатки к-т ( см. Ацидокомплексы), а также нейтральные молекулы, содержащие такие атомы, как О, N, Si, P, As или кратные связи, напр. Аммины), Н2О ( см. Акво-комплексы), СО ( см. Карбонилы металлов), амины, спирты, эфиры, олефины. [14]
Комплексообразование с карбамидом парафинов, составляющих высокоплавкие воски ( tnn 95 - 100 С), проводят в гомогенном растворе при повышенной температуре, что обеспечивает полноту протекания процесса. Раствор фильтруют, из фильтрата выделяют. [15]
Страницы: 1 2 3 4