Замедление - скорость - реакция
Cтраница 4
Гидрофилизация поверхности породы, эмульгирование и снижение вязкости нефти при добавлении бутанола позволяют, практически, сравнять скорости реакции соляной кислоты с карбонатной породой в водо - и нефтенасыщенной средах. При этом замена одноатомного спирта на многоатомный ( полигликоль, полиглицерин) приводит к полному блокированию реакции с нефтенасыщенной частью и значительному снижению скорости реакции с водонасыщенной, т.е. происходит замедление скорости реакции в углеводородном пласте. [46]
Рассмотренные теории позволяют очень просто объяснить явление отравления катализаторов [14] Вещества, являющиеся ядами для катализаторов гидрирования, обладают свободными единичными электронами или электронными парами и адсорбируются катализатором Образующаяся хемосорбцноииая связь настолько прочна, что обычно не разрывается в условиях реакции, вследствие чего активные центры прочно блокируются Для отравления катализаторов часто бывает достаточно очень небольшого количестпа иещества, гораздо мель глего, чем потребовалось бы для блокирования всех существующих активных центров. Это несоответствие подробно объяснено в мультнплетнои теории Если один из активных центров занят ингибитором, расстояние между остальными активными центрами становится слишком большим и в результате этого нарушается необходимое для реакции соответствие расстояния между активными центрами и размерами связей молекулы восстанавливаемого соединения Это выбывает замедление скорости реакции, а часто и ее полное торможение. Исследованиями отравления катализаторов доказано, что существует зависимость между эффективностью ядов для катализаторов и их строением. Кроме содержания ток сичного атома, который связывается с катализатором ( чаще всего сера, галоиды), большую роль играет величина нетоксичной части молекулы ингибитора, с ее увеличением возрастает токсичность соединения, так как она может прикрывать другие соседние активные центры. [47]
От других методов, поскольку при контакте активных масс с агрессивной водой в ней самопроизвольно устанавливается карбонатное равновесие. Такой метод стабилизации воды перспективен для небольших водоочистных комплексов, так как не требуется контроля процесса и сложного оборудования известкового хозяйства. Однако, замедление скорости реакции при низких температурах воды и невозможность получения воды с положительным индексом стабильности ( / 0 7) для создания защитной карбонатной пленки на поверхности трубопроводов ограничивают применение данного метода. [48]
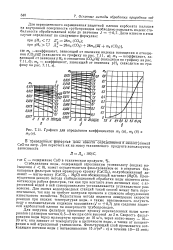 |
Графики для определения коэффициентов пц ( а, т2 ( б и / и3 ( в. [49] |
Преимуществом данного метода стабилизационной обработки воды является автоматическая работа фильтров, так как при контакте этих активных масс с агрессивной водой в ней самопроизвольно устанавливается углекислотное равновесие. Для малых водопроводных станций такой способ может быть перспективным, так как не требует контроля процесса и сложного оборудования известкового хозяйства. Недостатком метода является замедление скорости реакции при низких температурах воды, а также невозможность получить воду с положительным индексом насыщения ( J 0 7) для создания защитной карбонатной пленки на поверхности трубопроводов. [50]
Для достижения максимальной скорости реакции сульфохлорирования, а также оптимального соотношения хлора и серы необходима наименьшая интенсивность падающего света. Усиление интенсивности света не имеет влияния на ход реакции. Ниже наименьшей интенсивности света наблюдаются замедление скорости реакции и ухудшение соотношения хлора и серы, а хлорирование в углеродной цепи снова усиливается. При одинаковой интенсивности свет более коротких волн дает более низкое соотношение хлора и серы, чем длинноволновый свет. [51]
Наряду с явлениями катализа, характеризующимися увеличением скорости реакции, известны случаи, когда катализатор замедляет реакцию. Примером отрицательного катализа может служить замедление скорости реакции разложения перекиси водорода в присутствии незначительного количества серной кислоты. В данном процессе серная кислота играет роль отрицательного катализатора. [52]
Легко видеть, что если р стремится к единице, то скорость реакции при этом бесконечно убывает. Следовательно, точное Максвелл-Больц - дтповское распределение является в обсуждаемом случае принципиально невозможным. Приближенное равновесное распределение связано с большим замедлением скорости реакции. [53]
Применяют 50 - 200 мкМ раствор индикатора, объем которого составляет Vio или даже меньшую часть от объема испытуемого раствора. Титруют периодически, причем после каждой новой добавленной порции титрующего раствора встряхивают сосуд, в котором титруют, и наблюдают за окраской органической фазы. Приближение к конечной точке титрования делается заметным по замедлению скорости реакции, и поэтому следует более продолжительно встряхивать. Показателем конечной точки служит первое отчетливое изменение окраски индикатора, устойчивой после 30 сек. Индикаторная ошибка по большей части очень незначительна. Следует учитывать разрушающее влияние на дитизон повышенной температуры некоторых окислителей и прямых солнечных лучей. [54]
Исследование скорости окисления графита в различных временных интервалах и при различной температуре затруднено протеканием экзотермической реакции и значительными перепадами температур. Экспериментальные данные, приведены в табл. 38, указывают на замедление скорости реакции углерода с расплавом во времени. [55]
Страницы: 1 2 3 4