Молибденовый ангидрид
Cтраница 2
Получение молибденового ангидрида разложением молибденовокислого аммония, изучение его свойств. [16]
Переработка молибденового ангидрида начинается с растворения его в щелочи с небольшой добавкой перекиси водорода. Иногда растворению предшествует обработка МоОз азотной кислотой для окисления технеция, но присутствие нитратов может в дальнейшем ухудшить экстракцию, которая наряду с осаждением применяется для выделения технеция. [17]
По токсическим свойствам молибденовый ангидрид считается более ядовитым, чем металлический молибден. [18]
Окисел МоО3 - молибденовый ангидрид - представляет собой не растворимый в воде белый порошок, который при нагревании желтеет. В воде растворимы только молибдаты щелочных металлов; молибдаты других металлов растворяются только в щелочах. [19]
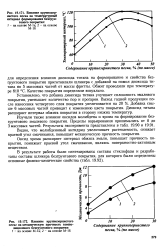 |
Влияние крупнозернистого песка на температурный интервал формирования безгрунтового покрытия.| Влияние крупнозернистого песка на механическую прочность композиционного безгрунтового покрытия. [20] |
Видно, что молибденовый ангидрид увеличивает растекаемость, снижает краевой угол смачивания, повышает механическую прочность покрытия. [21]
При этом молекулы молибденового ангидрида, обладая малым сродством к воде, соединяются друг с другом за счет дополнительных валентностей, и только те молекулы МоОз, которые находятся снаружи этого ядра, связаны с молекулами НгМоО4, образуя соединение типа HaMoCU МоОз, способное диссоциировать. [22]
Установлена степень использования молибденового ангидрида. [23]
Возгоночный способ получения молибденового ангидрида прост и не требует затрат реагентов. Однако прямое извлечение молибдена в готовый продукт низкое и будет тем ниже, чем больше в огарке примесей. Получающаяся этим способом трехокись молибдена очень тонкодисперсна, что создает значительные трудности для непосредственного ее использования при производстве молибденовых порошков восстановлением водородом. [24]
Несмотря па летучесть молибденового ангидрида, пасчет совпадает с опытом без ввсчеппя поправки на испарение молибденового ангидрида. По-видимому, в этих условиях он пе испаряется. [25]
При этом молекулы молибденового ангидрида, обладая малым сродством к воде, соединяются друг с другом за счет дополнительных валентностей, и только те молекулы МоОз, которые находятся снаружи этого ядра, связаны с молекулами Й2МоО4, образуя соединение типа ШМоСХ МоОз, способное диссоциировать. [26]
Однако при этой температуре молибденовый ангидрид обладает значительной летучестью. Кроме того, молибденовый ангидрид, получаемый из молибдата аммония, часто имеет синеватую, а в нижних слоях иногда даже коричневую окраску, вызванную образованием окислов пяти - и четырехвалентного молибдена. Это явление объясняется восстановительным действием аммиака, выделяющегося при реакции. [27]
Проведено исследование реакции восстановления молибденового ангидрида ( МоО3) германием. Установлено, что восстановление идет через образование летучей моноокиси германия. [28]
Для получения молибдена из молибденового ангидрида МоО8 на 100 г его берут 37 г алюминия и 50 г фторида кальция. Реакцию проводят в шамотовом тигле ( стр. [29]
Однако вследствие легкой испаряемости молибденового ангидрида образцы пужпо сначала прокаливать при 550 - 600 С в течение 3 - 4 ч с тем чтобы прошло восстановление молибденового ангидрида. Затем температуру постепенно повышают до 1200 - 1250 С и образцы выдерживают 3 - 4 ч п атмосфере азота. [30]
Страницы: 1 2 3 4