Изменение - валентное состояние
Cтраница 4
При слишком продолжительном перемешивании фаз экстракция в некоторых случаях может ухудшаться из-за разложения реагента и растворителя, изменения валентного состояния металла или изменения состава экстрагирующегося соединения. [46]
Из всего рассмотренного выше материала следует, что вся химия любого металла заключена в сравнительно узких границах изменения валентных состояний от 0 ( металлическое электронейтральное состояние) до положительнрй валентности ( зарядности), отвечающей, как правило ( но, разумеется, с исключениями), номеру группы периодической системы. [47]
Таким образом, очевидно, что инициирование цепей солями переменной валентности в реакциях окисления тесно связано с изменением валентного состояния металлов. [48]
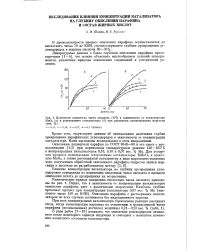 |
Изменение кислотных чисел оксидата ( КЧ в зависимости от концентрации МпСЬ ( а и растворимого катализатора ( б при различных концентрациях марганца ( вес. %. [49] |
В ряде работ [7-10] показано, что окисление углеводородов начинается после некоторого периода индукции и совпадает с моментом изменения валентного состояния катализатора. [50]
Она указывает, что авторы необоснованно приписывают различие магнитного момента окрашенных железом борных и безборных эмалей и стекол, изменению валентного состояния ионов железа. Кроме того, находясь в положении модификатора решетки, железо вследствие амфотерности проявляет кислотные или основные свойства в зависимости от составов стекол. Еще менее вероятно, что при нагревании стекла до 500 - 700 возможно существенное изменение валентного состояния железа, которым авторы объясняют наблюдавшиеся изменения магнитного момента. Это различие следует приписать изменению координационного состояния ионов железа, а не их валентного состояния. Это подтверждает также изменение окраски стекол с железом при нагревании. При этом стекла с железом приобретают ярко-желтую окраску, в то время как переход в двухвалентное состояние вызвал бы потемнение окраски за счет поглощения иона Fea в красной части спектра. [51]
При сравнении активности некоторых оксидов металлов замечено, что она возрастает с понижением энергии связи кислорода, которая зависит от легкости изменения валентного состояния катиона металла в оксиде, определяемого его электронной структурой. Отсюда вытекает возможность регулирования каталитической активности оксидных катализаторов путем введения добавок. Добавка оксидов, содержащих более электроотрицательный катион, уменьшает энергию связи кислорода и соответственно повышает каталитическую активность, причем последняя возрастает с увеличением порядкового номера промотирующего металла. [52]
При сравнении активности некоторых окислов металлов замечено, что она возрастает с понижением энергии связи кислорода, которая зависит от легкости изменения валентного состояния катиона металла в окисле, определяемого его электронной структурой. Отсюда вытекает возможность регулирования каталитической активности окисных катализаторов путем введения добавок. Добавка окислов, содержащих более электроотрицательный катион, уменьшает энергию связи кислорода и соответственно повышает каталитическую активность, причем последняя возрастает с увеличением порядкового номера промотирующего металла. [53]
Страницы: 1 2 3 4