Ион - металл
Cтраница 3
Ионы металлов в каждом случае образуют гранецентрированную кубическую решетку. [31]
Ионы металлов, более электроотрицательных, чем серебро, определению не мешают. [32]
 |
Фрагмент кристаллической решетки ферроцнанида типа M. fZj, [ Fe ( CN8 ] 2 ( V8 часть элементарной ячейки. [33] |
Ионы металла или Н30, находящиеся в структурных пустотах. Функция: обмен на ионы металлов раствора. [34]
Ионы металлов, извлеченных из разбавленных растворов на адсорбци-онно-комплексообразовательной колонке, могут быть де-сорбированы небольшим объемом подходящего реагента и таким образом сконцентрированы в несколько десятков и сотен раз. Наиболее подходящими десорбентами являются сильные кислоты, смещающие равновесия ( 202) и ( 207) в сторону разложения комплексов. [35]
Ионы металлов, обладающих магнитными свойствами ( железо, никель), легко разряжаются на ртутном катоде, и образовавшиеся мелкодисперсные частицы металлов под действием магнитного поля осаждаются на поверхности ртути. Эти частицы металлов, имеющие низкое перенапряжение для выделения водорода, становятся центрами образования вязкой массы, называемой амальгамным маслом. [36]
Ионы металлов Pt2, Pd2, Au3 и Cu2 образуют почти исключительно плоские квадратные структуры, в то время как для Ni2, Co2, Fe2 и Мп2 структуры этого типа вообще встречаются гораздо реже и в приведенном ряду металлов распространенность плоских структур снижается. В ковалентных плоских квадратных хелатах этих металлов предпочтительна конфигурация со спаренными электронами ( - гибридизация), поэтому они представляют собой диамагнитные соединения, например бис - ( диметилглиоксимато) никель. Для комплексов этого типа менее характерно присоединение дополнительных лигандов, таких, как пиридин или аммиак, с образованием октаэдрических структур. И наоборот, полярный, тетраэдрический парамагнитный бис - ( ацетилацето-нато) никель очень легко реагирует с пиридином, образуя октаэдриче-ский аддукт. [37]
Ионы металлов, у которых первая координационная сфера полностью заполнена, могут образовывать и вторую ( внешнюю) координационную сферу. [38]
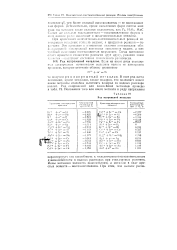 |
Ряд напряжений металлов. [39] |
Ионы металлов являются окислителями, а металлы в виде простых веществ - восстановителями. [40]
Ионы металлов находятся в водных растворах в виде акво-комплексов. Окислительно-восстановительные потенциалы простых ионов по существу неизвестны, и имеющиеся данные относятся к аквокомплексам, в которых лигандом является вода. На величину окислительно-восстановительного потенциала образующего иона большое влияние оказывает химическая природа лигандов. [41]
Ионы металлов в титруемом растворе могут образовывать комплексы с подходящими лигандами. Например, в аммиачном буферном растворе многие ионы металлов образуют аммиакаты; в ацетатном буферном растворе - ацетатные комплексы. При достаточно высокой концентрации ионов гидроксила образуются гидроксожомплексы. [42]
Ионы металлов в титруемом растворе могут образовывать комплексы с подходящими лигандами. Например, в аммиачном буферном растворе многие ионы металлов образуют аммиакаты; в ацетатном буферном растворе - ацетатные комплексы. При достаточно высокой концентрации гидроксид-ионов образуются гидроксокомплексы. [43]
Ионы металлов, суль фиды которых растворимы в воде, подразделяются в свою очередь на ионы, осаждаемые и не осаждаемые карбонатом аммония. [44]
Ионы металла, имеющие положительный заряд, проникая в раствор электролита, совершают работу, перемещаясь в поле потенциала границы раздела металл - электролит, затрачивая энергию. Эта энергия компенсируется работой изотермического расширения от большей концентрации ионов на поверхности к меньшей в растворе. [45]
Страницы: 1 2 3 4