Свободный ион
Cтраница 4
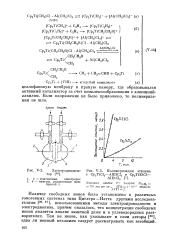 |
Электродиализа - [ IMAGE ] - 3. Полимеризация этилена. [46] |
Наличие свободных ионов было установлено в различных гомогенных системах типа Циглера-Натта другими исследователями I38 37 ], использовавшими методы электропроводности и электродиализа, причем оказалось, что концентрация свободных ионов является вполне заметной даже и в углеводородных растворителях. Тем не менее, как указывают и сами авторы [33], едва ли ионный механизм следует рассматривать как всеобщий. [47]
Присутствие свободного иона Mg2 в эфирном растворе кажется маловероятным вследствие малой диэлектрической постоянной растворителя. Металлический магний, осаждающийся при электролизе эквимолекулярной смеси ( C2H5) 2Mg и Mg28Br2, нерадиоактивен. [48]
У свободного иона все пять функций (2.4) эквивалентны, так как им соответствует одно и то же значение энергии. Поэтому если ( Zz) 0 для состояний, которые описываются функциями (2.4), то отсюда еще не следует, что z - компонента орбитального момента в данном случае действительно равна нулю, поскольку такой результат зависит только от выбора представления. В противоположность этому, функции (2.4) иона в кубическом кристаллическом поле образуют две различные неэквивалентные группы, принадлежащие de - и - состояниям, энергия которых различна. Состояния электронов, которые описываются этими функциями, различаются z - компонентами орбитального момента l z mfi, т О, 1 и формально соответствуют состоянию р-электрона в свободном атоме. [49]
Наличие свободных ионов в растворах электролитов подтверждается следующими фактами. [50]
Для свободных ионов магнитные свойства определяются зеемановским расщеплением эффективного спинового дублета. И, как известно [6.33], в этом случае энергия этого расщепления определяется не самим тензором д -, а его сверткой вида Gij dikdjk которая является симметричным тензором. [51]
Число свободных ионов н электронов в диэлектриках чрезвычайно мало, поэтому их электропроводность незначительна и обусловлена преимущественно подвижностью макромолекул или их частей, определяющих, в свою очередь, подвижность ионов. [52]
Концентрации свободных ионов РиО и Fe2 приблизительно равны стехиометрическим концентрациям, поскольку константы гидролиза этих ионов малы по сравнению с концентрацией Н - ИОНОБ. [53]
Концентрацию свободных ионов железа можно представить ( как это было сделано на стр. [54]
Страницы: 1 2 3 4