Атом - кислород
Cтраница 3
Атом кислорода более электроотрицателен, чем атом азота, он прочнее удерживает свои неподеленные электроны, труднее отдает их в сопряженную систему; поэтому гидроксигруппа является более слабым ЭД-заместителем, чем аминогруппа. [31]
Атом кислорода, входящий в состав гетероцикла, повышает цвет ( см. разд. [32]
Атомы кислорода имеют во внешнем слое 6 электронов и радиус атома 0 6 А. [33]
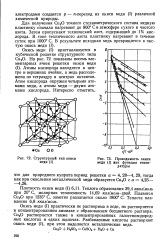 |
Структурный тип окиси меди ( I.| Проводимость окиси меди ( I как функция температуры. [34] |
Атомы кислорода находятся в центре и вершинах ячейки, а медь расположена по тетраэдру в центрах октантов. Атом кислорода окружен четырьмя атомами меди, а атомы меди - двумя атомами кислорода. [35]
Атом кислорода, связанный с углеродом двойной связью, оттягивает электроны в свою сторону. Углерод приобретает некоторый положительный заряд и притягивает электроны второго атома кислорода из группы - ОН, что приводит к сдвигу электронного облака связи О - Н в направлении кислорода. [36]
Атом кислорода имеет на втором энергетическом уровне два непарных электрона и две электронные пары, которые в соединениях кислорода могут оставаться как неподеленные. Одна из них может быть представлена для образования координационной связи. [37]
Атомы кислорода не существуют в виде положительных ионов, они не могут отдавать свои электроны другим элементам. По отношению к кислороду все другие элементы всегда проявляют положительную валентность. [38]
 |
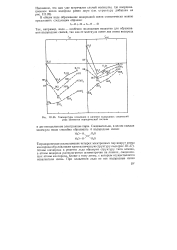
Углеводороды ( а - в и производные углеводородов, содержащие N, S, О или С1 ( г - е. [39] |
Атомы кислорода, серы и азота, обладающие свойствами неметаллов, склонны к образованию ковалентных связей. Они могут занять место углерода в цепи или цикле. Углы связей для этих атомов почти такие же, как и для атомов углерода, поэтому заметного напряжения в цепи при такой замене не наблюдается. [40]
Атом кислорода в спиртах связан с атомом водорода и с радикалом. В зависимости от характера радикала спирты реагируют с разрывом связи между водородом и кислородом или между радикалом и кислородом. [41]
Атом кислорода имеет два неспарениых электрона и две неподеленные электронные пары, что указывает на способность кислорода образовывать четыре ковалентные связи. [42]
Атомы кислорода в оксиэтиленовых группах подобных веществ обладают способностью образовывать продукты присоединения. Присоединение молекул воды делает оксиэтилированные соединения растворимыми в воде, а взаимодействие с молекулами красителя объясняет их поведение при крашении. Под действием сил, обусловливающих ассоциацию, молекулы оксиэтилирован-ных веществ образуют агрегаты, что является причиной аномальной вязкости их водных растворов. [43]
Атом кислорода, например, образует две ординарные связи в молекуле воды или двойную связь в молекуле кислорода. Аналогично и для азота: три ординарные связи в молекуле аммиака либо тройная связь в молекуле азота. [44]
 |
Температуры плавления и кипения водородных соединений ряда элементов периодической системы. [45] |
Страницы: 1 2 3 4 5