Механизм - реакция - нитрование
Cтраница 2
Вопрос о механизме реакции нитрования уже давно является предметом многочисленных исследований. [16]
В чем состоит механизм реакции нитрования и окислительного действия азотной кислоты. [17]
Изучались главным образом механизмы реакции нитрования предельных углеводородов азотной кислотой, двуокисью азота и азотным ангидридом; механизм нитрования других кляссмз соединений мало исследован. [18]
Оригинальную точку зрения на механизм реакции нитрования ароматических соединений выдвигает в своих работах французский исследователь Ланц. Он рассматривает нитрование как процесс, связанный с кислотно-основным равновесием в системе, исходя при этом из представлений Бренстедта. [19]
Кинетические измерения значительно способствовали выяснению механизма реакции нитрования. [20]
Титовым и др. При изучении механизма реакции нитрования непредельных соединений окислами азота было установлено, что двуокись азота присоединяется, подобно галоидам, по двойной связи, давая динитропродукты. [21]
Автором настоящей книги выдвинута следующая трактовка механизма реакции нитрования ароматических соединений неорганическими нитратами в присутствии А1С1з, сближающая эту реакцию с реакцией Фриделя - Крафтса. [22]
Автором настоящей книги выдвинута следующая трактовка механизма реакции нитрования ароматических соединений неорганическими нитратами в присутствии А1С13, сближающая эту реакцию с реакцией Фриделя-Крафтса. [23]
Автором настоящей книги выдвинута следующая трактовка механизма реакции нитрования ароматических соединений неорганическими нитратами в присутствии А1С1з, сближающая эту реакцию с реакцией Фриделя - Крафтса. [24]
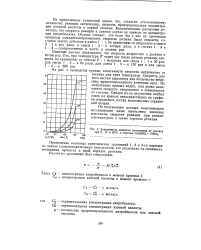 |
Зависимость скорости нитрования от состава при 0, 10 и 20 С в системе CeH5NO2 - HNO3. [25] |
Из приведенных уравнений видно, что, согласно установленному механизму реакции нитрования, скорость пропорциональна концентрации азотной кислоты в первой степени. Кинетическими расчетами показано, что скорость реакции в данном случае не зависит от концентрации нитробензола. Отсюда следует, что если бы у нас не протекали процессы комплексообразования, скорость должна была возрасти, согласно закону действия в смеси 1; I, по сравнению со скоростью в смеси 2: 1 в два раза, в смеси 1: 2 - в четыре раза, а в смесях 1: 3 и 1: 4 - соответственно в шесть и восемь раз. [26]
Многочисленные ( подчас и противоречивые) работы по вопросу о механизме реакции нитрования разбросаны по страницам советской и иностранной журнальной литературы, что в значительной мере затрудняет ознакомление с ними. Поэтому ниже, в отдельной главе, нами систематизированы основные работы по механизму нитрования ароматических соединений. [27]
Ряд проведенных исследований по нитрованию ароматических соединений в различных органических растворителях мало продвинул вопрос о механизме реакции нитрования, так как не был установлен даже кинетический порядок реакции. Бенфолд и Инголд [2] нашли, что при применении большого избытка азотной кислоты с нитрометаном в качестве растворителя такие реакционноспособные соединения, как бензол, толуол и этилбензол, нитровались с одинаковой скоростью согласно закону для реакций нулевого порядка. [28]
Для определения количества указанных кислот с целью контроля степени чистоты 3 3 - ДНДФС и выяснения механизма реакции нитрования дифенилсульфона применен спектрофотометрический метод, основанный на различии их спектров поглощения в нейтральной или щелочной средах в области 300 - 450 им. [29]
Ввиду того что процессы нитрования, происходящие довольно легко, часто приводят к смеси различных нитропродуктов а также к продуктам окисления при неполном использовании азотной кислоты, для химиков всегда представляли интерес вопросы о механизме реакций нитрования. [30]
Страницы: 1 2 3