Парциальный молярный объем
Cтраница 3
Относительное постоянство парциального молярного объема Si02 при изменении состава ( см. табл. 36) не находит количественного объяснения на основе предлагаемой структуры дискретных ионов. [31]
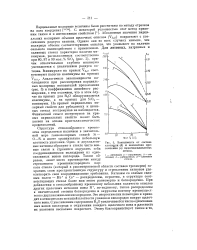 |
Зависимость от состава. [32] |
Абсолютные значения парциальных молярных объемов щелочных окислов ( VR2o) возрастают с увеличением радиуса катиона. Однако они во всех случаях меньше, чем молярные объемы соответствующих окислов, что указывает на наличие сильного взаимодействия с кремнеземом. Для литиевых, натриевых и калиевых стекол характерно наличие минимумов, расположенных соответственно при 80, 87 и 90 мол. Минимумам на кривых VRjo соответствуют пологие максимумы на кривых Vsio2 - Аналогичные закономерности наблюдаются при рассмотрении парциальных молярных показателей преломления ( рис. 3) и коэффициентов линейного расширения, с тем отличием, что в этом случае на кривых для R20 обнаруживаются максимумы, а на кривых для Si02 - минимумы. На кривых парциальных молярных свойств для рубидиевых и цезие-вых стекол экстремумов не наблюдается. Физический смысл экстремумов на кривых парциальных свойств может быть уяснен на основе кристаллохимических представлений. [33]
Как правило, парциальные молярные объемы в области малых концентраций слабо зависят от последней, поэтому AF представляет собой почти постоянную величину, а поправка линейно увеличивается с ростом концентрации и обусловливает верхний концентрационный предел этого метода измерения чисел переноса. Справедливость поправки на изменение объема была доказана экспериментально ( [30], стр. Довольно затруднительно привести пример величины этой поправки, так как на ее значение сильно влияет природа системы. [34]
Ниже приведены величины парциального молярного объема азота в смеси азота ( 40 %) с водородом при 0 С. [35]
Если ряд растворителей имеет примерно одинаковые парциальные молярные объемы, то величина осмотического давления является мерой сродства. [36]
Отмечается, что зависимость парциального молярного объема водорода ич давления прямолинейна. [37]
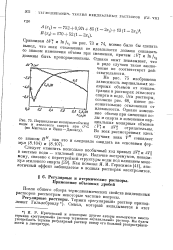 |
Парциальные молярные объемы. [38] |
На рис. 75 изображена завртсимость парциальных молярных объемов от концентрации в растворах этилового спирта в воде. Эти растворы, согласно рис. 68, имеют положительные отклонения от идеальности. [39]
Соотношение, предложенное для определения парциального молярного объема при бесконечном разбавлении для газов при низких значениях приведенной температуры15, дает удовлетворительные результаты; при отсутствии других данных это соотношение, вероятно, будет самым точным для большинства случаев. [40]
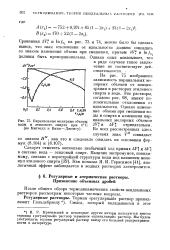 |
Парциальные молярные объемы. [41] |
На рис. 75 изображена зависимость парциальных молярных объемов от концентрации в растворах этилового спирта в воде. Эти растворы, согласно рис. 68, имеют положительные отклонения от идеальности. [42]
Соотношение, предложенное для определения парциального молярного объема при бесконечном разбавлении для газов при низких значениях приведенной температуры 15, дает удовлетворительные результаты; при отсутствии других данных это соотношение, вероятно, будет самым точным для большинства случаев. [43]
 |
Зависимость энтальпии перехода моля воды из водного раствора NaCI в чистую жидкую воду от температуры. [44] |
Сеченова от давления через зависимость парциального молярного объема растворенного компонента от концентрации электролита. [45]
Страницы: 1 2 3 4