Окись
Cтраница 2
Окись Sc2O3 - белый, в кислотах медленно растворимый порошок. Его соли бесцветны, не дают спектра поглощения. Безводный ScCl3 еще неизвестен Сернокислая соль Sc2 ( SO) 3 кристаллизуется с 6 № О. Ее двойная соль: 3K2SOJSc2 ( SO4) 3 нерастворима в растворе KaSO4 Щавелевая кислота осаждает из растворов щавелевокислую соль Sc2 ( C2O4) s6H2O в виде белого, мелкокристаллического осадка. Спектр искры хлористого соединения дает более 100 линий часть которых очень блестяща. [16]
Окись и закись азота практически не растворимы в воде. [17]
Окиси трехвалентного Ni и Со трех - и четырехвалентного Мп выделяют при кипячении с разбавленной соляной кислотой хлор, который легко узнается по запаху. [18]
Окиси ( эпоксиды) являются очень напряженными трехчленными циклами; их способность к реакциям присоединения близка к реакционной способности двойных связей олефинов. Поэтому равновесие цикл полимер практически полностью сдвинуто в сторону образования полимера. В зависимости от характера инициирования и условий реакции эпоксиды полимеризуются по ступенчатому или цепному механизму. При катионной полимеризации эпоксидов получаются полимеры с низкой молекулярной массой. При анионной полимеризации эпоксидов получаются более высокомолекулярные полимеры. [19]
Окись лантена La203 имеет температуру плавления около 2300 С, обладает способностью к гидратации на воздухе, подобно окиси кгльция, поэтому она не представляет интереса как сырье для получения керамики чистых окислов. [20]
Окись гадолиния - белого цвета, поглощает углекислоту из воздуха, темнеет при нагревании, гигроскопична, растворяется в кислотах. [21]
Окиси обычно восстанавливаются медленно при многочасовом кипячении в эфире. [22]
Окиси, содержащие галоген, в ходе восстановления часто дега-логенируются. [23]
Окиси образуются из транс-тритерпеноидных и стероидных бромгидринов в результате обработки их щелочью. [24]
Окиси расщепляются дибораном относительно медленно, причем расходуется 1 гидридный эквивалент. [25]
Окись ] 100; в этих условиях в растворе существуют только енолят-анионы. [26]
Окись Sc2O3 получают, прокаливая гидроокись, карбонат, сульфат, нитрат, оксалат скандия. В воде практически не растворяется, плохо растворяется в холодных разбавленных кислотах и очень хорошо - в концентрированных. [27]
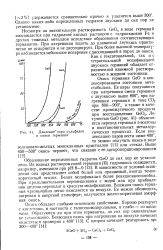 |
Давление пара сульфидов и окиси германия. [28] |
Окись обладает слабыми основными свойствами. Хорошо реагирует с кислотами, в частности с галогеноводородными, и слабо - со щелочами. Образуются ли при этом германиты, до сих пор окончательнс не установлено. [29]
Окись углерод а называется также угарным газом; получается при неполном сгорании углерода от недостаточности воздуха или температуры в топке. [30]
Страницы: 1 2 3 4