Отношение - растворимость
Cтраница 2
В отношении растворимости сильных электролитов С. С. Чин вывел два правила. [16]
К равна отношению растворимостей обеих сернокислых солей. [17]
 |
Простейшие приборы для возгонки. [18] |
Величина К равна отношению растворимостей вещества в обоих растворителях. Различие между этими величинами определяется главным образом взаимной растворимостью обоих растворителей. Теоретически коэффициент распределения не зависит от концентрации, однако в реальных растворах наблюдаются отклонения от этого правила, иногда довольно значительные. [19]
Не только в отношении растворимости, но и в отношении температур плавления существует периодичность в гомологическом ряду: кислоты с четным числом атомов углерода плавятся при более высокой температуре, чем с нечетным. В противоположность жирным одноосновным кислотам температуры плавления двухосновных кислот понижаются с увеличением молекулярного веса, по крайней мере в ряду кислот с четным числом углеродных атомов. [20]
Не только в отношении растворимости, по и в отношении температур плавления существует периодичность в гомологическом ряду: кис-лены с четным числом атомов углерода плавятся при более высокой температуре, чем с нечетным. В противоположность жирным одноосновным кислотам температуры плавления двухосновных кислот понижаются с увеличением молекулярного веса, по крайней мере в ряду кислот с четным числом углеродных атомов. [21]
Данные [7] в отношении растворимости индия в б - Pu являются, по-види-мому, завышенными. [22]
Константа распределения приблизительно равна отношению растворимостей вещества в индивидуальных фазах. [23]
Константа распределения приблизительно равна отношению растворимостей экстрагируемого вещества в отдельных фазах. Необходимо только помнить, что при экстракции обе фазы взаимно насыщаются друг другом. [24]
Константа распределения приблизительно равна отношению растворимостей экстрагируемого вещества в индивидуальных фазах. [25]
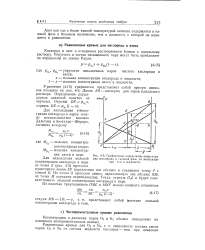 |
Графическое определение концентрации кислорода в газовой фазе по концентрации его в жидкости. [26] |
Кислород и азот в отношении растворимости близки к идеальному раствору. [27]
Отмечаются серьезные различия в отношении растворимости водорода между сталями разных классов. [28]
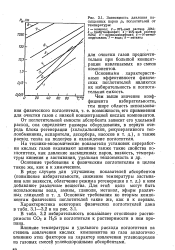 |
Зависимость давления насыщенных паров ра поглотителей от температуры. [29] |
В табл. 3.2 избирательность показывает отношение растворимости СО2 и H2S в поглотителе к растворимости в нем пропана. [30]
Страницы: 1 2 3 4