Отношение - растворимость
Cтраница 3
Между тем при кислотном восстановлении отношение растворимости обратное. Образовавшаяся аминогруппа вызывает усиленную растворимость соединения при малой даже концентрации водородных ионов, и если имеются другие восстановляющиеся группы, они могут быть также легко вовлечены во взаимодействие с восстановителем. [31]
Константа распределения, вычисленная как отношение растворимости гомологов в обоих растворителях, увеличивается при Q-GS в н-алкиле, при дальнейшем увеличении числа атомов углерода рост Р0 замедляется и, возможно, приостанавливается. [32]
Возможно близкое к нулю значение отношения растворимостей основного вещества и примеси. [33]
Константа распределения вещества часто равна отношению растворимостей его в обеих фазах. Факторы, влияющие на растворимость вещества в той или иной фазе, отражаются и на его распределении. Есть ряд веществ, которые уменьшают или увеличивают растворимость органических соединений в водной или органической фазах. Это обстоятельство дает возможность влиять на распределение вещества между двумя фазами. [34]
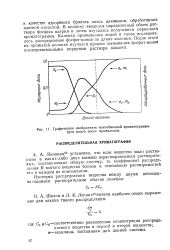 |
Графическое изображение ионообменной хроматограммы трех ионов после проявления. [35] |
К взятого вещества близок к отношению растворимостей его в каждом из компонентов. [36]
Коэффициент распределения К приближенно пропорционален отношению растворимостей ПАВ в водной и масляной фазах. [37]
Поведение перхлоратов и гексафторфосфатов в отношении растворимости идентично, однако в кристаллографическом отношении эти соли не являются аналогами. [38]
Это же справедливо и в отношении растворимости. Константы диссоциации характеризуют свойства молекул в растворе, и поэтому равенство этих констант для dl - и / - кислот свидетельствует о том, что энантиомеры обладают одинаковой кислотностью. Химические свойства также не зависят от кристаллической формы, вследствие чего d -, I-и / - кислоты одинаково реагируют с одним и тем же реагентом, причем во всех трех случаях реакции протекают с одинаковой скоростью. Способность одной из кислот вращать плоскость поляризации света вправо ( а другой - влево) связана с асимметрией молекулы, и характер этой связи до конца еще не выяснен, но вполне понятно, что зеркально изомерные вещества должны обладать равной по величине и противоположной по знаку оптической активностью. [39]
Оно может быть решено в отношении растворимости подстановкой различных значений плотности и температуры. [40]
Правило Руффа утверждает, что если отношение растворимостей кристаллизанта и примеси больше единицы, то твердая фаза обогащается примесью, если же меньше - то обедняется. Это правило, согласно данным, приведенным на рис. 8.8, выполняется при равновесии с точностью до полупорядка. [41]
Согласно данным работы [ 21, отношение растворимости мелких частиц одного и того же размера ( L. Этими различиями в растворимости, а следовательно, и в микропересыщении, объясняются в значительной мере формы выпадающих осадков ( микрокристаллы у BaSO4, коагулированный коллоид у AgaCrO4) и степени их полидисперсности. [42]
Константа распределения Р соединения приблизительно равна отношению растворимостей этого соединения в органической и водной фазах. Следовательно, экстрагироваться может только такое соединение, которое слабо растворимо в воде, но легко растворяется в органических растворителях. [43]
К - коэффициент распределения, равный отношению растворимости веществ в насыщенном паре и в воде, из которой он образуется. [44]
Наблюдаемый в некоторых случаях параллелизм между отношениями растворимостей макро - и микрокомпонентов является скорее исключением, чем правилом. Отсюда следует, что действительное значение коэффициента пропорциональности / в уравнении ( 16 - 2) должно совпадать со значением константы фракционирования, физический смысл которой был выяснен нами ранее. [45]
Страницы: 1 2 3 4