Переход - кислота
Cтраница 2
Что касается образования бензаминовой кислоты, то можно представить себе два различных пути: если выразить, вместе с Мульдером, состав нитробензиновой кислоты рациональной формулой Ci4H804 N2O3 Н20, то в нашей водной кислоте оказывается тот же радикал CuHsOi в соединении с аммиаком. Надо, следовательно, принять, что при переходе нитробензиновой кислоты в бензаминовую эквивалент воды отщепляет один эквивалент азотистой кислоты. Если же принять для нитробензиновой кислоты формулу Ci4Hs03 N204 HaO, то для образования из нее бензаминовой достаточно представить себе, что N204 замещается на N2H4 или собственно 04 на Н4 без выделения воды. [16]
Наиболее сильными ацилирующими агентами являются хлоран-гидриды и ангидриды, а у солей это свойство практически отсутствует. Этим же рядом, но справа налево, определяется возможность взаимного превращения производных кислот: переход кислоты в эфир обратим, а при образовании амидов равновесие почти полностью смещено в их сторону. [17]
Обнаружено удивительное многообразие фактов, характеризующих механизм экстракции кислот и коэффициенты их распределения. Чтобы разобраться в этом обилии фактов, важно знать энергетические характеристики не только суммарных реакций перехода кислоты из водного раствора в органический, но главным образом энергетические характеристики отдельных стадий экстракционного процесса. Известна только одна работа [34], в которой определены изобарные потенциалы, энтальпии и энтропии суммарных реакций экстракции азотной кислоты из водного раствора различными органофосфорными соединениями. [18]
Для определения урана в более кислых растворах необходимо соответственно повысить концентрацию буферной смеси в растворе высаливателя, так как в противном случае рН водной фазы может оказаться настолько низким, что комплексен III не будет оказывать маскирующего действия на мешающие примеси. Кроме того, высокая концентрация кислоты в исходном анализируемом растворе может мешать последующему определению урана вследствие перехода кислоты в органическую фазу, а затем в реэкстракт, рН которого может снижаться ниже допустимого значения ( ниже 1 5 для арсеназо III или ниже 0 5 для хлорфосфоназо III), что приведет к неполному связыванию урана в окрашенный комплекс. [19]
При достаточно высоком значении рН практически все количество кислоты находится в ионизированном состоянии, ь этом случае переход кислоты в слой органического растворителя практически невозможен. [20]
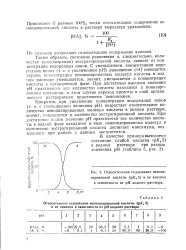 |
Относительное содержание неионизированной кислоты ( р / С а 5 и ее анионов в зависимости от рН водного раствора. [21] |
При достаточно высоком значении рН практически все количество кислоты находится в ионизированном состоянии, в этом случае переход кислоты в слой органического растворителя практически невозможен. [22]
Как отмечалось выше, для четкого разделения кислот с помощью ИЭРХ необходимо, чтобы элюент содержал разбавленную хлористоводородную кислоту, которая обеспечивает переход кислот и их анионов в молекулярную форму. [23]
Из рассмотрения этого механизма следует, что реакция сильно замедляется как в очень кислых, так и в очень щелочных средах. В сильнокислых средах скорость реакции падает, так как почти весь семикарбазид превращается в неактивную сопряженную кислоту, а в сильнощелочных средах реакция тормозится из-за перехода кислоты НА в ее неактивное сопряженное основание. [24]
Однако небольшие количества оставшегося нитробензола могут загрязнить конечный продукт реакции и часто являются причиной того, что после осаждения из щелочного раствора кислота выделяется в виде масла. Во время вторичной отгонки, к которой, во избежание вспенивания, следует приступать с осторожностью, удаляют по следяне следы растворителя, причем кислота переходит в раствор в виде натриевой соли, а нейтральны продукты реакции и окись алюминия остаются нерястворенными. Переход кислоты в содовый раствор часто происходит недостаточно легко ввиду окклюзии окиси алюминия, а также в том случае, если не производится перегонка с паром. [25]
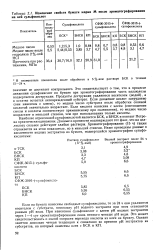 |
Изменение свойств бумаги марки М после хроматографирования на ней сульфокислот. [26] |
Если на бумагу нанесены свободные сульфокислоты, то за 24 ч они удаляются носителем с субстрата, поскольку рН водного экстракта при этом становится равным рН воды. Это может свидетельствовать о малой скорости перехода кислоты из клея на бумагу. Однако заметна довольно четкая тенденция к снижению во времени рН экстрактов из субстратов, на который нанесены клеи с БСК и КП. [27]
Исходя из сказанного выше, целесообразно производить окисление церия озоном при возможно более высокой концентрации азотной кислоты. Перед экстракцией нитрометаном необходимо разбавить раствор до 4 9 - 5 3 N по азотной кислоте и вести экстракцию нитрометаном, приведенным в равновесие с азотной кислотой указанной концентрации. При этом в процессе экстракции должен происходить вначале некоторый переход кислоты из водного раствора в нитрометан ( в связи с высаливающим действием нитрата церия), затем, по мере снижения концентрации соли-обратный переход кислоты из органической фазы в водную. [28]
Исходя из сказанного выше, целесообразно производить окисление церия озоном при возможно более высокой концентрации азотной кислоты. Перед экстракцией нитрометаном необходимо разбавить раствор до 4 9 - 5 3 N по азотной кислоте и вести экстракцию нитрометаном, приведенным в равновесие с азотной кислотой указанной концентрации. При этом в процессе экстракции должен происходить вначале некоторый переход кислоты из водного раствора в нитрометан ( в связи с высаливающим действием нитрата церия), затем, по мере снижения концентрации соли-обратный переход кислоты из органической фазы в водную. [29]
При чтении справа налево это же уравнение изображает присоединение протона к основанию, которое переходит в сопряженную с ним кислоту. Однако, протоны не существуют в водных растворах в свободном виде, поэтому реакция (1.18) не может протекать изолированно. Необходимо присутствие одновременно другого основания, которое, присоединяя протон, превращается в кислоту. Обратная реакция перехода кислоты в основание также требует непременного присутствия другой кислоты, доставляющей протон с переходом в сопряженное основание. [30]
Страницы: 1 2 3