Протекание - процесс - коррозия
Cтраница 1
Протекание процесса коррозии во времени может происходить ускоренно, равномерно или замедленно ( фиг. [1]
На протекание процесса коррозии оказывает также влияние скорость потока морской воды. [2]
Вероятность протекания процессов коррозии с водородной деполяризацией при повышении рН уменьшается. Для такого важного в техническом отношении материала, как железо, она становится при рН5 пренебрежительно малой. [3]
Скорость протекания процесса коррозии у различных металлов и сплавов ( при прочих равных условиях) неодинакова, и по се величине судят о коррозионной стойкости металла. [4]
 |
Диаграммы, иллюстрирующие правило Таммана. [5] |
Характер протекания процесса коррозии в основном определяется анионным составом раствора. Однако в ряде случаев на ход процесса оказывают влияние и катионы. Ионы, присутствующие в коррозионной среде, принято делить на активаторы и ингибиторы ( замедлители) коррозии. [6]
Схема протекания процесса коррозии железа во влажном воздухе, загрязненном хлороводородом, аналогична схеме, изображенной на рис. 102, только со следующими отличиями: анодом ( разъедаемыми участками) являются участки, лишенные естественной окисной пассивирующей пленки, а катодом - участки, покрытые пленкой. Коррозия протекает в пленке влаги, адсорбированной поверхностью ме1 - талла и содержащей растворенный кислород. [7]
В протекании процесса коррозии под действием окислов железа и меди определенное значение имеет разность тепловых нагрузок и температур между соседними участками металла, на которых находится окисножелезный шлам. [8]
При протекании процесса коррозии в нейтральных средах концентрация углерода в сталях и чугунах не влияет на его скорость. [9]
При протекании процессов коррозии потери металла с поверхности вызывают уменьшение поперечного сечения образца и пропорциональное возрастание его электросопротивления, по приросту которого и можно судить о размере коррозии. Метод измеренния скорости коррозии по изменению электросопротивления образцов основан на том, что продукты коррозии имеют электропроводность на несколько порядков меньшую, чем металл, и, следовательно, любой процесс ионизации и выхода иона в раствор будет вызывать возрастание электросопротивления исследуемого образца. [10]
В результате протекания процессов коррозии и осмоления смазочного масла образуются смолообразные агрегаты и осадки. Для предотвращения образования таких агрегатов или их разрушения, применяют добавки, образующие с ними устойчивые дисперсии. В патенте показано, что одноза-мещенные литиевые соли алифатических углеводородзамещенных производных янтарных кислот или ангидридов янтарных кислот могут реагировать с органическими гидроксисоединениями, давая эффективные малозольные ингибиторы коррозии. [11]
 |
Потенциостати-ческая поляризационная. [12] |
В случае протекания процесса коррозии с водородной деполяризацией количество растворенного металла пропорционально количеству выделившегося водорода, что позволяет определить скорость коррозии по количеству выделившегося водорода. [13]
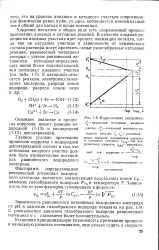 |
Коррозионная диаграмма. [14] |
Главное условие протекания процессов коррозии с ( водородной деполяризацией состоит в том, что потенциал анодного участка должен быть отрицательнее потенциала раанювесного водородного электрода. [15]
Страницы: 1 2 3 4