Прочность - связь - кислород
Cтраница 3
Поскольку исследования изотопного обмена были проведены лишь на небольшом количестве окислов, природу и прочность связи кислорода в окислах следует оценивать и с помощью других параметров. [32]
 |
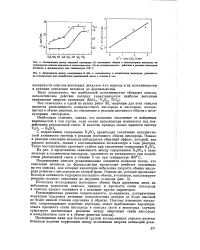
Сравнение раскислительнои способности алюминия и титана в железе и в сплаве железо - хром ( 18 % при 1600. [33] |
Такое явление объясняется увеличением прочности сил связи кислорода в расплаве, содержащем хром по сравнению с прочностью связи кислорода в жидком железе. [34]
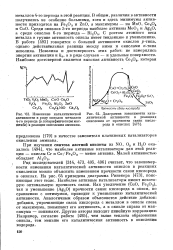
Ряд исследователей [314, 473, 495, 496] считает, что закономерности изменения каталитической активности окислов в реакциях окисления можно объяснить изменением прочности связи кислорода в окислах. На рис. 64 приведена диаграмма Ринекера [473], поясняющая этот тезис. Наиболее активные катализаторы имеют некоторую оптимальную прочность связи. Как увеличение ( CuO, Fe203), так и уменьшение ( Ag20) прочности связи кислорода в окиси, по сравнению с оптимумом, приводит к уменьшению каталитической активности. Аналогичным образом объясняется действие добавок: добавки, упрочняющие связь кислорода с металлом в окисле слева от максимума, повышают его активность, а в окисле справа от максимума - понижают. Другие авторы находят линейную корреляцию Например, согласно работе [495], чем выше теплота образования окисла, тем меньше его каталитическая активность в окислении водорода. [36]
В соответствии с изложенными представлениями следовало ожидать, что увеличение радиуса центрального атома аниона должно сопровождаться уменьшением прочности связи кислорода и, как следствие, - увеличением скорости изотопного обмена. Уменьшение валентности центрального атома также должно вызывать ослабление монолитности аниона. На примерах изучения изотопного обмена газообразного кислорода с молибдатом и карбонатом натрия эти представления были подтверждены. Для молибдата натрия степень обмена, равная 18 0 %, была достигнута за 7 час. Больший радиус атома молибдена в анионе МоС) 4 - и меньшая валентность углерода в анионе С0з - по сравнению с серой из аниона SC4 - имеют следствием увеличение подвижности кислорода в реакциях обмена, что свидетельствует о меньшей прочности связи кислорода в Na2Mo04 и NaaCOs по сравнению с соответствующим сульфатом. [37]
Ед-величина, постоянная для определенной группы веществ; х 0 5; ДЯ-теплота реакции, отнесенная к одному молю прореагировавшего кислорода; g - прочность связи кислорода, определяемая из температурной зависимости давления кислорода над поверхностью оксида. [38]
Было проведено сопоставление каталитической активности исследованных катализаторов с температурой максимумов скорости десорбции кислорода ( табл. 2), определенной по методике, аналогичной [7], что может характеризовать прочность связи кислорода с катализатором. [39]
Желая получить продукт неполного окисления, нужно обеспечить достаточно высокую скорость его образования и в то же время стабилизировать его на поверхности, чтобы предотвратить дальнейшее окисление. Выполнение этих требований существенно зависит от прочности связи кислорода с катализатором. [40]
Известны и другие корреляции между особенностью кристаллической структуры и склонностью простых оксидон к стеклооб-разовапию. Сап предположил, что весьма важной хараЕстеристи - кой является прочность связи кислорода с другими элементами. Он обратил внимание на то, что энергия связи в стсклооб разующих оксидах составляет 330 кДж / моль, в то время как энергия связи кислорода с ионами модификаторов, которые не участвуют в образовании сетчатой структуры, существенно меньше. [41]
В то же время естественно предположить, что в ряду окислов различных металлов изменение обеих величин дй и д0 определяется главным образом изменением природы катиона, и это подтверждается существованием приблизительно линейной зависимости между этими величинами. Поэтому для большинства окислов корреляционные зависимости между каталитической активностью и прочностью связи кислорода, полученные в работах Борескова с сотрудниками и в наших работах, аналогичны. [42]
 |
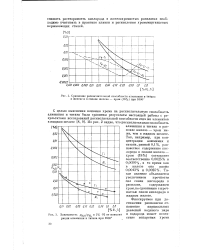
Связь каталитической активности А окислов металлов с числом незаполненных d - уровней в катионах решетки. [43] |
Для ряда процессов образующийся кислород-углеводородный комплекс должен изомеризоваться. Направление изомеризации, которое определяет состав продуктов реакции, зависит от прочности связи кислорода и углеводородного радикала. [44]
Механизм действия смешанных катализаторов пока неясен. Ринекер [5] предполагает, что каталитическая активность таких систем связана либо с изменением прочности связи кислорода в кристаллической решетке вследствие образования новых соединений из окислов, либо обусловлена изменением числа электронов или дырок в кристаллах. Благодаря этому на смешанных контактах изменяются скорости лимитирующих донорных или акцепторных стадий. [45]
Страницы: 1 2 3 4