Величина - константа - равновесие
Cтраница 2
Величина константы равновесия показывает, что со стороны статики нет препятствий для полного вытеснения водорода магнием из хлористого водорода, если даже парциальное давление водорода в газовой фазе будет равно 1 атм. [16]
Величина константы равновесия этой реакций составляет около Ю4, что вполне достаточно для проведения титрования по методу вытеснения. После завершения реакции обоих металлов с комплексоном происходит также скачок pMg, несмотря на то, что Mg2 - noH связывается в комплекс скорее, чем Ва2 - ион ( см. стр. [17]
Величина константы равновесия, пропорциональная четвертой степени парциального давления оставшегося хлористого водорода, показывает, что это давление имеет преобладающее значение. Влияние упругости водяного пара менее заметно; что же касается содержания кислорода, то оно еще менее влияет на ход реакции, и потому вместо кислорода можно при сжигании хлористого водорода с теми же результатами применять воздух. [18]
Величины констант равновесия, вычисленные по уравнению Гапона и Ванселоу, или увеличиваются или уменьшаются с изменением отношения количеств обменивающихся катионов в твердой фазе. [19]
Величина константы равновесия зависит от природы реагирующих веществ я от температуры. [20]
Величины константы равновесия должны быть известны, и должны быть известны способы их определения из энергий Гиббса образования компонентов. [21]
Величина константы равновесия / Ср указывает на молярные соотношения реагирующих веществ в состоянии равновесия. Чем больше / Ср, тем глубже протекает реакция; при достаточно большой величине / Ср реакция практически может идти до конца. [22]
Величины константы равновесия должны быть известны, и должны быть известны способы их определения из энергий Гиббса образования компонентов. [23]
Величина константы равновесия, а следовательно, и степень термической диссоциации быстро возрастают с температурой. [24]
Величина константы равновесия указывает, что количественное протекание реакции наиболее вероятно в щелочной среде. [25]
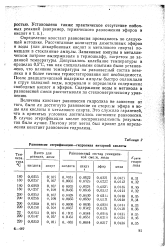 |
Равновесие этерификации-гидролиза янтарной кислоты. [26] |
Величины констант равновесия гидролиза не зависели от того, было ли достигнуто равновесие со стороны эфира и воды или кислоты и метилового спирта. Это служило гарантией, что в принятых условиях достигалось состояние равновесия. [27]
Величина константы равновесия дитизоната цинка в хлороформе равна приблизительно 3 ( стр. [28]
Величина константы равновесия последней реакции показывает, что равновесие сдвинуто лишь немного вправо и что только небольшая часть кадмия может выделиться в виде металла. При этом кадмий может выделиться только после полного восстановления двухвалентной меди до металла. Если бы случайно выделился металлический кадмий, то он немедленно, как показывает опыт, вытеснил бы эквивалентное количество меди. [29]
Величина константы равновесия межфазного обмена определяется изменением свободной энергии в соответствии с уравнением - r KosM-& G / RT. Последняя обусловлена затратой энергии на пересольватацию ионов при переходе из фазы в фазу и разностью энергий ассоциации ионов в органической фазе. [30]
Страницы: 1 2 3