Раствор - окислитель
Cтраница 3
В процессе титрования раствором окислителя восстановленная форма анализируемого вещества переходит в окисленную форму с изменением потенциала системы. В точке эквивалентности анализируемое вещество полностью переходит в окисленную форму и происходит резкое изменение потенциала ( рис. IV. Такой скачок потенциала свидетельствует о достижении точки эквивалентности. [31]
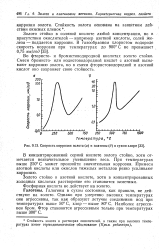 |
Скорость коррозии золота ( а и платины ( б в сухом хлоре. [32] |
Стойкость золота в растворах окислителей, а также при высоких температурах имеет термодинамическое обоснование ( Прим. [33]
В отсутствие в растворе окислителей процесс называется обычным и при их наличии - ускоренным. [34]
 |
Разрядные кривые медно-маг. [35] |
При отсутствии в растворе окислителей, которые могут окислять ионы Mg без выделения водорода, преобладает окисление их водой. Этим объясняется постоянная потеря 40 - 50 % металла, наблюдаемая при работе элементов. [36]
При отсутствии в растворе окислителя иридий осаждается не сразу. Возможно, что радикал хлороиридата, подобно хлороплатинату, гидролизуется медленно. В осадке, выделяющемся в присутствии бромата, иридий находится в более высокой степени окисления, чем четырехвалентная. [37]
При наличии в растворе окислителя, способного перевести металл в высшую степень окисления, процесс становится каталитическим и ион металла играет роль переносчика электронов от водорода к окислителю. [38]
При отсутствии в растворе окислителя иридий осаждается не сразу. Возможно, что радикал хлороиридата, подобно хлороплатинату, гидродизуется медленно. В осадке, выделяющемся в присутствии бромата, иридий находится в более высокой степени окисления, чем четырехвалентная. [39]
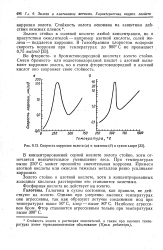 |
Скорость коррозии золота ( а и платины ( б в сухом хлоре. [40] |
Стойкость золота в растворах окислителей, а также при высоких температурах имеет термодинамическое обоснование ( Прим. [41]
Стойкость серебра в растворах несильных окислителей, а также стойкость против окисления при высоких температурах имеет термодинамическое объяснение. [42]
При погружении электрода в раствор окислителя или восстановителя он отдает или принимает электроны. Электрод будет заряжаться положительно или отрицательно до определенного потенциала, уравновешивающего стремление электронов к перераспределению, причем положительный заряд электрода становится тем выше, чем сильнее окислительные свойства раствора. Потенциал, до которого заряжается электрод при погружении его в данный раствор, является мерой окислительной активности последнего. Его называют электродным окислительным потенциалом раствора. [43]
В качестве титранта используются растворы окислителей и восстановителей. [44]
 |
Прибор для ебнаружения SO2, ионов. [45] |
Страницы: 1 2 3 4