Растворение
Cтраница 3
Растворение Ai2 ( SO4) s в воде производят в реакторе / при температуре 60 - 90 СС. Суспензию носителя насосом 4 подают на фильтр-пресс 5 для фильтрования и промывки геля. [31]
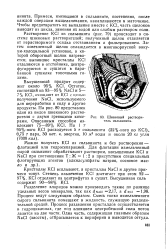 |
Шнековый растворитель сильвинита. [32] |
Растворение КС1 из сильвинита ( рис. 79) происходит в си-г стем. Затем осветленный щелок охлаждается в многокорпусной вакуум-холодильной установке, в которой оборотный щелок нагревается; выпавшие кристаллы КС1 отделяются в отстойнике, центрифугируются и сушатся в барабанной сушилке топочными газами. [33]
Растворение их в водных растворах минеральных кислот, щелочей, цианидов, аммиака возможно только в присутствии окислителей. [34]
Растворение проводится в азотной кислоте ( одна часть HNOs уд. Сначала действуют на все количество алюминия и пиролюзита одной третью необходимого количества HNO3 и добавляют при этом / з никеля. Растворение проводится при нагревании и перемешивании. Нерастворившаяся часть алюминия и перекиси марганца растворяется со второй третью никеля и азотной кислоты. [35]
Растворение обычно сопровождается тепловым эффектом, что в принципе влияет на интенсивность внешней массоотдачи. Оценки [2] показывают, что температура поверхности растворяющейся частицы может повышаться на несколько градусов. [36]
Растворение друг в друге веществ, ассоциированных посредством водородных связей, может привести либо к распаду последних, либо к образованию новых связей. Так, при растворении спирта в воде водородные связи в воде и спирте могут разрушиться. [37]
Растворение 8Оз в воде сопровождается выделением теплоты. [38]
Растворение какого из указанных ниже веществ в воде должно оказать наибольшее влияние на коллигативные свойства полученного раствора. [39]
 |
Газовые пипетки и отбор пробы газа с их помощью. [40] |
Растворение проводят в стакане или в конической колбе при нагревании на песочной бане или на электроплитке. Для уменьшения выпаривания кислоты стакан или колбу накрывают часовым стеклом. [41]
Растворение следует считать законченным, когда нерастворимый остаток, образовавшийся на дне стакана или колбы, взмучивается при взбалтывании раствора и медленно оседает на дно. Нерастворимый остаток при растворении руд состоит главным образом из диоксида кремния ( SiO2) серо-беловатого цвета. Если в нерастворимом остатке имеются черные частицы, которые хрустят при надавливании стеклянной палочкой и не размельчаются, это указывает на то, что растворение еще не закончено. [42]
Растворение и выщелачивание твердых веществ часто проводится в аппаратах с отражательными перегородками или в гладко-стенных аппаратах, снабженных турбинными мешалками. Процесс выщелачивания рассматривается на стр. [43]
Растворение в воде ускоряется при употреблении теплой ( 60 - 70) воды. Для быстрого приготовления водных растворов указанной концентрации рекомендуется вести растворение фуразонала в теплой воде ( 60 - 70), а затем предоставить полученному раствору принять комнатную температуру. Препарат не изменяется при длительном ( около часа) кипячении его водных растворов. [44]
Растворение в воде слабой кислоты, например уксусной НАс, не сводится просто к НАс. При этом НАс является кислотой - донором протона, тогда как НаО является основанием - акцептором протона. Поскольку происходит и обратная реакция, ион оксония является кислотой, а ацетатный ион - основанием. Уксусная кислота и ион ацетата называются сопряженной кислотно-основной парой, так же как и вода и ион оксония. Кислотами или основаниями могут быть как нейтральные молекулы, так и катионы и анионы. Помимо рассмотренных выше равновесий, NHt и HSC4 могут считаться примерами кислот, a Fe ( H2O) sOH2f - примером основания ( см. стр. Некоторые молекулы или ионы могут и акцептировать и отдавать протоны; они называются амфотерными. Наглядными примерами такого поведения являются вода и ион бисульфата. [45]
Страницы: 1 2 3 4