Фотохимическая система
Cтраница 2
Очень сложная смесь продуктов последующих реакций RNO в обычной фотохимической системе сильно затрудняет кинетические исследования. В дальнейшем окись азота может служить окислителем или катализировать термический распад некоторых соединений. Поэтому возникает вопрос о том, соответствует ли минимум скорости ингибирования при увеличении давления окиси азота полному ингибированшо или же просто одинаковой эффективности обрыва и инициирования цепей. [16]
 |
Модель структуры хлоропласта. [17] |
Как указывалось выше, фотосинтез происходит в двух фотохимических системах. Проблема пространственной локализации этих систем в хлоропластах очень актуальна. [18]
Определение интенсивности поглощаемого света и квантовых выходов в фотохимических системах с помощью термоэлементов предполагает введение еще одной дополнительной поправки на отражение и рассеяние света на окошках реакционного сосуда ( см. разд. [19]
Фундаментальные различия в фотохимии этих двух спектроскопических состояний необходимо учитывать при рассмотрении фотохимических систем. Однако нужно помнить о том, что я - я - возбуждение не обязательно означает, что делокализация возбуждения в я я - состоянии будет важнейшим фактором, определяющим фотохимию системы. Так, облучение спиртовых растворов бензофенона при 2537 А первоначально приводит к 1 ( я я) - состоя-нию бензофенона, однако продукты реакции и их квантовые выходы практически те же самые, что и при облучении светом 3660 А, где происходит п - - я - поглощение. Это понятно, если предположить, что я - я - погло-щение, приводящее к состоянию S2, сопровождается быстрой внутренней конверсией в состояние Si i ( n n), которое затем подвергается безызлуча-тельной интеркомбинационной конверсии, приводящей к состоянию Ti 3 ( гс я), идентичному реакционноспособному триплету, образующемуся при 3660 А. [20]
Было бы наивным предполагать, что единственной функцией кислорода, введенного в фотохимическую систему, является реакция со свободными радикалами, получившимися в первичных фотохимических процессах. Однако существуют фотохимические системы, в которых кислород используется для направления первичного процесса в определенную сторону. Кислород практически не влияет на внутримолекулярные первичные процессы фотораспада, идущие без участия свободных радикалов или триплет-ных возбужденных состояний. Если известно, что квантовый выход данного продукта практически не зависит от давления кислорода, то это является сильным доказательством того, что данный продукт образуется в первичном акте, вероятно при фотораспаде возбужденного синглетного состояния, хотя возможно также и короткоживущее триплетное состояние. Эти продукты образуются в первичном акте, вероятно, из синглетного возбужденного состояния ( или очень короткоживущего триплетного), а свободные радикалы не играют заметной роли. [21]
Изучая кинетику фотохимических реакций, можно получить важные данные о механизме реакции, однако имеется свойственная только фотохимическим системам трудность, которую необходимо учитывать. Могут существовать значительные различия между измеряемыми скоростями реакции и локальными скоростями реакции, если не принять соответствующих мер предосторожности. [22]
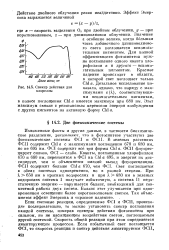 |
Спектр действия для казало, однако, что наряду с мак. [23] |
Изложенные факты и другие данные, в частности биохимическое разделение, доказывают, что в фотосинтезе участвуют две фотохимические системы ФС1 и ФСП. В зеленых растениях ФСП содержит СЫ а с максимумами поглощения 670 и 680 нм, но не 695 нм. [24]
Было бы наивным предполагать, что единственной функцией кислорода, введенного в фотохимическую систему, является реакция со свободными радикалами, получившимися в первичных фотохимических процессах. Однако существуют фотохимические системы, в которых кислород используется для направления первичного процесса в определенную сторону. Кислород практически не влияет на внутримолекулярные первичные процессы фотораспада, идущие без участия свободных радикалов или триплет-ных возбужденных состояний. Если известно, что квантовый выход данного продукта практически не зависит от давления кислорода, то это является сильным доказательством того, что данный продукт образуется в первичном акте, вероятно при фотораспаде возбужденного синглетного состояния, хотя возможно также и короткоживущее триплетное состояние. Эти продукты образуются в первичном акте, вероятно, из синглетного возбужденного состояния ( или очень короткоживущего триплетного), а свободные радикалы не играют заметной роли. [25]
При поглощении веществом импульсной вспышки высокой интенсивности образуется относительно высокая концентрация свободных радикалов или промежуточных частиц, которые могут быть обнаружены спектроскопически. Импульсный фотолиз является хорошим средством изучения первичных процессов в фотохимических системах ( разд. Имеются три основных группы импульсных систем: 1) электрический разряд между металлическими электродами в газе при низком давлении; 2) искровой разряд большой энергии между электродами из магния или другого относительно летучего металла; 3) вспышка взрывающейся проволочки. Сначала рассмотрим первый из этих методов, который используется наиболее широко. [26]
Квантовый выход продукта нетрудно измерить. Число падающих квантов света можно измерить специальным прибором, называемым актинометром, который представляет собой стандартную фотохимическую систему с известным квантовым выходом. Квантовый выход дает ценную информацию о фотохимической реакции. Так, если квантовый выход продукта - конечная величина, не меняющаяся при изменении условий эксперимента, продукт, по всей вероятности, образуется в результате первичного процесса, который и определяет скорость. Если квантовый выход продукта превышает единицу ( в некоторых случаях он доходит до 1000), это указывает на цепную реакцию. [27]
В данном разделе были рассмотрены главным образом скорости свободных радикалов и молекул, пришедших в состояние термического равновесия. Однако теория скоростей реакций представляет большой интерес при описании реакций электронно-возбужденных молекул, образующихся в фотохимических системах. Имеются существенные различия между системами, активированными фотохимически и термически. Основное различие состоит в распределении колебательной энергии реагента по состояниям. [28]
Однородность и пропускание продажных стеклянных фильтров не всегда соответствуют указанным в проспектах фирм-изготовителей. Поэтому действительное пропускание фильтра необходимо определять экспериментально для того участка, который подвергается воздействию света в фотохимической системе, где он используется. [29]
Наиболее типичным методом проведения экспериментов с временным разрешением в фотохимии является метод импульсного фотолиза. Этот метод первоначально разработали Нор-риш и Портер в 50 - е годы нашего века с целью идентификации промежуточных продуктов реакции в фотохимических системах. Стационарные концентрации промежуточных продуктов - атомов, радикалов или возбужденных соединений, - имеющиеся в стационарных условиях, обычно слишком малы для того, чтобы зарегистрировать их по спектрам поглощения. Однако при использовании импульсного источника света предельно высокой интенсивности удается получить концентрации короткожи-вущих промежуточных соединений, достаточные для спектроскопического наблюдения. [30]
Страницы: 1 2 3 4