Галогензамещенное соединение
Cтраница 2
Заместители в ароматическом или гетероциклическом ядре, с одной стороны, облегчают, а с другой - затрудняют прямое нитрование. Влияние метальных групп сравнительно мало заметно; сильнее влияние более длинных цепей, причем в этом случае особенно сильно проявляется окисляющее действие азотной кислоты. Наибольшей реакционной способностью обладают фенолы и амины, а также галогензамещенные соединения. Напротив, трудно нитруются карбоновые кислоты, сульфэкислотыисами нитросоеди-нения. В отношении образования изомеров найдены не наблюдаемые в других случаях отклонения и закономерности. [16]
При применении концентрированной серной кислоты образование простого эфира может происходить также через стадию кислого алкилсульфата. Здесь наряду с другими реакциями, при которых в спиртовом растворе образуются электрон-недостаточные частицы, рассматриваются и оба указанных типа реакций. К реакциям подобного типа, кроме дегидрирования, относятся также реакции ионизации реакционноспособных галогензамещенных соединений, реакции протонирования олефинов и некоторых карбонилсодержащих соединений, реакции разложения диазосоединений в присутствии спирта, а также довольно специфичная реакция получения а-гало-генэфиров путем присоединения спиртов к карбонильным соединениям в присутствии галогеноводородов. [17]
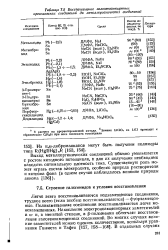 |
Восстановление галогенвамеырнкых, органических, соединений до металлорганических соединений. [18] |
Легче всего восстанавливаются иодзамещенные соединения, труднее всего ( если вообще восстанавливаются) - фторзамещсн-ные. Полизамещенные соединения восстанавливаются легче мо-нозамещенных. Накопление электроноакцепторных заместителей в а - и, в меньшей степени, в р-положении облегчает восстановление галогензамещенных соединений. [19]
Обычным путем через р - кетоэфиры эти продукты получаются с трудом. Для простых алкильных групп выходы 2-алкилкетонов бывают посредственными, за исключением р-тетралона, для которого получаются высокие выходы. Енамин, образующийся из пирролидина, обладает наибольшей, а енамин из морфолина - наименьшей нукле-офильной способностью по отношению к атаке галогензамещенных соединений. Если N-алкилирование представляет затруднения, ал-килирование енамина N. N-дициклогексиламина может пойти в основном по углероду. Полярные растворители, например ацетонитрил, более эффективно промотируют алкилирование, чем неполярные. [20]
Вторым типом ионизационного детектора является детектор электронного захвата. Образующиеся ионы собирают и измеряют их концентрацию с помощью электродов, усилительная же система подобна той, которую используют в пламенно-ионизационном детекторе. Однако принцип действия в этом случае значительно отличается тем, что зоны растворенного анализируемого вещества обнаруживают по вызываемому ими уменьшению постоянного ионного тока. Это уменьшение связано с тем, что степень ионизации резко зависит от концентрации свободных электронов в детекторе, а некоторые химические частицы чрезвычайно эффективно захватывают свободные электроны. Минимально обнаруживаемый поток пробы для веществ с высоким сродством к электрону, например для галогензамещенных соединений, около 10 - 13 г / с, и этот детектор, таким образом, значительно более чувствителен для таких частиц, чем пламенно-ионизационный детектор. Детекторы электронного захвата чувствительны к соединениям, содержащим галогены, фосфор, свинец или кремний, а также к полиядерным ароматическим соединениям, нитросоединениям и некоторым кетонам. Пестициды, например, содержат фосфор или хлор, поэтому этот детектор идеально подходит для измерения низких уровней этих соединений. Можно также вводить атомы галогенов в соединения, к которым этот детектор не чувствителен. Например, кислоты можно этерифицировать фторированными спиртами, а спирты и амины обработать фторангидридами кислот. [21]
Ферпосон [83] получил постоянный выход флуоресценции при уменьшении длины волны возбуждающего света от 3600 до 2200 А для антрацена, пирена, хризена, 1 2-бензантрацена, азулена и 9 10-дихлорантрацена. Однако для 9 10-дибромантрацена выход флуоресценции уменьшается примерно наполовину при 3050 А, затем остается постоянным на протяжении всего второго перехода, а потом вновь падает. Это позволяет предполагать, что внутренняя конверсия S2 - Si проходит достаточно медленно и переход ( под влиянием тяжелых атомов) в триплетное состояние из S2 имеет большую вероятность, чем переход из Si. Дальнейшее падение выхода может объясняться предиссоциацией связи С - Вг. Выход фосфоресценции остается постоянным на протяжении всей области возбуждения St и S2 для нафталина и его галогензамещенных соединений, за исключением иодпроизвод-ного, для которого выход уменьшается при длинах волн короче 3200 А. Этот эффект объясняется, по-видимому, разрывом связи С-I, так как соответствующее сплошное поглощение имеет максимум около 2600 А. Такого рода эксперименты были проведены с раствором или с твердыми стеклами. Фергюсон и др. [50, 57] установили, что интенсивность флуоресценции некоторых ароматических соединений, особенно тетрацена, в кристаллическом состоянии возрастает при охлаждении. Однако это возрастание почти наверняка вызвано ослаблением межмолекулярной миграции энергии, которая растрачивает электронную энергию на колебания решетки. [22]
Этот метод имеет более существенное значение для получения фенолов ( гл. Это и есть хорошо известный метод определения метоксигруппы по Цейзелю. Он более удобен в то1м случае, если в реакции затрагиваются атомы галогена. Чтобы исключить такую возможность, галоген замещают на довольно - мало реакционноспособную алкоксигруппу, которую на последней стадии синтеза вновь превращают в исходное галогензамещенное соединение. [23]
Катализатор является наименее контролируемым фактором анализа, поэтому следует периодически проверять его работу по известному соединению. Первые несколько проб после установки нового катализатора могут не дать хороших результатов. В новом приборе для определения углеродного скелета срок жизни катализатора может быть 1 - 2 сут. Срок жизни катализатора в приборе, который находился в эксплуатации в течение нескольких месяцев, может быть 2 - 3 нед, при этом с одним и тем же катализатором можно провести 50 - 100 анализов. При введении на катализатор нелетучих соединений ( полимеры, масла) его активность может уменьшиться. Активность катализатора быстрее уменьшается при повышенных температурах; при 350 С может произойти резкое уменьшение активности в течение суток. Активность катализатора уменьшается и при анализе галогензамещенных соединений, так как эти соединения образуют галогеноводороды; небольшое число анализов малых количеств этих соединений может не принести вреда, но, как было указано выше, чрезмерное количество этих кислот на катализаторе может вызывать нежелательное разрушение углерод-углеродных связей. [24]
Страницы: 1 2