Состояние - равновесие
Cтраница 4
Состояние равновесия наступает при достижении адиабатного распределения параметров в сопловом сечении вихревой трубы. [46]
 |
Условия термодинамического равновесия. [47] |
Состояние равновесия характеризуется при постоянных внешних условиях неизменностью параметров во времени и отсутствием в системе потоков. Состояния, не удовлетворяющие данному определению, называются неравновесными. [48]
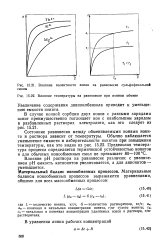 |
Влияние валентности ионов на равновесие сульфофенольной смолы.| Влияние температуры на равновесие при ионном обмене. [49] |
Состояние равновесия между обмениваемыми ионами ионита и раствора зависит от температуры. Обычно наблюдается уменьшение емкости и избирательности ионитов при повышении температуры, как это видно из рис. 15.22. Предельная температура процесса определяется термической устойчивостью ионитов и для обычных ионообменных смол не превышает 80 - 100 С. [50]
Состояние равновесия между твердыми частицами и разделяющей жидкой прослойкой описывается фундаментальными уравнениями поверхностного слоя ( см. раздел V. В методе избытков реальная система сравнивается с идеализированной, где экстенсивные величины относятся к сосуществующим объемным фазам. [51]
Состояние равновесия не зависит от относительных количеств фаз. [52]
Состояние равновесия реализуется только при определенном сочетании значений параметров, характеризующих систему. [53]
Состояние равновесия характеризуется правилом, фаз Гиббса, которое определяет связь между числом степеней свободы системы, числом ее компонентов и числом фаз. [54]
Состояние равновесия подчиняется правилу фаз Гиббса, сущность которого излагается в курсе физической химии. [55]
Состояние равновесия и скорость ее определяются температурой, давлением, соотношением аммиака и диоксида углерода и содержанием воды в реакционной смеси. [56]
Страницы: 1 2 3 4