Газообразное состояние - вещество
Cтраница 2
Для газообразного состояния вещества, согласно закону Авогадро, при постоянной температуре и давлении количество атомов в единице объема постоянно. [16]
Разновидность газообразного состояния вещества; отличается тем, что может находиться в равновесии с тем же веществом в конденсированном состоянии. [17]
Различают капельно-жидкое и газообразное состояния вещества. К а п е л ь н о-ж и д к и м называется состояние, отличающееся почти полной несжимаемостью тела и весьма малой его температурной расширяемостью; плотность капельно-жидких тел остается почти неизменной, не зависящей от давления и температуры. [18]
Под газообразным состоянием вещества понимается такое его состояние, которое характеризуется значительной подвижностью частиц. Вещество в газообразном состоянии вследствие большой подвижности молекул газа не может иметь определенного объема и формы; оно занимает всегда весь объем и имеет форму сосуда, в котором находится. [19]
Под газообразным состоянием вещества понимается такое его состояние, которое характеризуется значительной подвижностью частиц. Вещество в газообразном состоянии вследствие большой подвижности молекул газа не может иметь определенного объема и формы: оно занимает всегда весь объем и имеет форму сосуда, в котором находится. [20]
 |
Адиабатическое расши рение газа в пустоту. [21] |
В газообразном состоянии вещества внутренняя энергия сравнительно просто может быть определена экспериментально. Для этого достаточно исследовать адиабатическое расширение газа в пустоту. Впервые такой опыт был проведен Гей-Люссаком, а затем Джоулем. [22]
Характерной особенностью газообразного состояния вещества является то, что между его молекулами практически отсутствуют силы взаимного притяжения. [23]
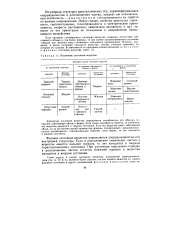 |
Различные состояния вещества. [24] |
Если признаки газообразного состояния вещества очевидны ( отсутствие собственного объема и, тем более, формы), то при оценке конденсированного состояния ( твердое или жидкое) могут возникнуть кажущиеся противоречия. Поэтому, указывая, в каком состоянии находится вещество, следует уточнять признаки, по которым это сделано. [25]
Что касается газообразного состояния веществ при низких плотностях ( при ш40), то эта единая обобщающая зависимость, как видно из рисунка, не соблюдается. [26]
И действительно, газообразное состояние вещества является примером существующего в природе полного, совершенного беспорядка во взаимном расположении и движении частиц. Нет такого микроскопа, который позволил бы увидеть движение газовых молекул, но, несмотря на это, физики могут достаточно детально описать жизнь этого невидимого мира. [27]
Часть СТ изображает собой газообразное состояние вещества. Точка С соответствует состоянию насыщения, линия СгО измеряет давление насыщенного пара. Чем далее мы отходим от точки С в сторону возрастающих объемов, тем более наша кривая приближается к равносторонней гиперболе. Часть кривой AQ изображает жидкое состояние вещества, действительно здесь, мы знаем, давление растет чрезвычайно быстро при малейшем уменьшении объема, поэтому изотерма в этой части своей поднимается почти параллельно оси ординат. Точки этого прямолинейного отрезка не о изображаются уравнением ( 57) Ван-дер - Ваальса, которое относится лишь к однородному состоянию вещества. Для состояний, промежуточных между точками А и С, уравнение Ван-дер - Ваальса дает волнообразную кривую ANBMC. И эта часть кривой имеет глубокий физический интерес. Отрезок AN изображает малоустойчивые состояния перегретой жидкости ( см. ниже); отрезок СМ - также весьма мало устойчивые состояния пересыщенного пара. При очень чистом веществе и больших предосторожностях эти малоустойчивые состояния, предвиденные теорией, могут быть и осуществляемы на опыте. Наконец, пунктированный отрезок изотермы MBN изображает собою совсем неустойчивые состояния вещества, которые именно вследствие своей неустойчивости не могут просуществовать и самого короткого времени, а поэтому и не могут быть наблюдаемы. Что эти состояния, действительно, вполне неустойчивы, - станет нам ясно, если мы обратим внимание на то, что в этой части кривой давление возрастает вместе с увеличением объема и, наоборот, падает при уменьшении объема. [28]
В отличие от газообразного состояния вещества, в жидкостях, вследствие весьма большой концентрации молекул, происходит образование отдельных неустойчивых молекулярных структур. Образование молекулярных структур в жидкости усиливается по мере фазового перехода вещества из жидкого состояния в твердое. Наличие молекулярных структур в жидкостях приводит к тому, что молекулярное трение при течении жидкостей по сравнению с газами оказывается значительно большим. Динамическая вязкость у жидкостей больше, чем у газов. Однако вследствие значительно большей плотности жидкостей кинематическая вязкость у жидкостей меньше, чем у газов. [29]
Изотермы в области газообразного состояния вещества представляют собой кривые, имеющие вблизи кривой насыщения положительный угловой коэффициент и обращенные выпуклостью вверх. [30]
Страницы: 1 2 3 4