Строение
Cтраница 3
Строение этих ионов не описано здесь в деталях, но указана литература по кристаллическим структурам их солей. Длины связей N-S и N-О близки к 1 73 и 1 43 А соответственно, за исключением специально оговоренных случаев. [31]
Строение Со ( Ме3РО) 2 ( МО3) 2 может быть также описано как тетраэдри-ческое, если рассматривать бидентатный NO3 в качестве единого лиганда; оптические и магнитные свойства этой молекулы ( а также иона Co ( NO3) 42 -) подтверждают мысль о том, что атом металла находится в тетраэдрическом поле лигандов. [32]
 |
Фосфорные оксокислоты. [33] |
Строение, да и само существование мета - и пирофосфористоп кислот все еще пе установлены достоверно. [34]
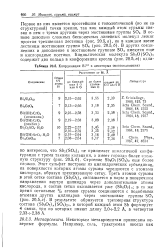 |
Координация В1Ш в некоторых оксосоединениях. [35] |
Строение Sb6O7 ( SO4) 2 еще более сложно. Этот сульфат построен из цилиндрических субъединиц, на поверхности которых атомы сурьмы чередуются с атомами кислорода, образуя трехсвязанную сетку. В результате образуется трехмерная структура состава ( SbgOr SC bn, в которой каждый атом Sb формирует 4 связи, три из которых имеют длину 2 0 - - 2 2 А, а четвертая 2 33 - 2 38 А. [36]
Строение этих соединений при нормальном давлении ( НД) и давлении 40 кбар и температуре 1000 С ( ВД) сопоставлено ниже. Вторая ВД-модпфикация BaSi2 получена при 600 - 800 С н давлении 40 кбар. Фазы ВД в течение нескольких месяцев устойчивы также при нормальных давлении н температуре в отсутствие воздуха и влаги; при нагревании до 400 С они переходят в фазы НД. [37]
Строение двух из трех полиморфных модификаций Hg3S2Cl2 определено вполне надежно. В а-форме сетка трехмерная ( разд. [38]
Строение кристаллических SnFi [11] и SnF2 ( CH3) 2 [12] описано в гл. [39]
Строение упорядоченной и разупорядоченпой фаз показано на рис. 29.9. Атомы расположены в узлах ОЦК-ре-шетки в одном случае упорядоченным образом, в другом - статистически. [40]
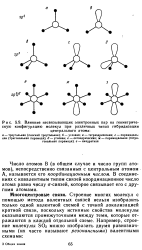 |
Влияние несвязывающих электронных пар на геометрическую конфигурацию молекул при различных типах гибридизации. [41] |
Строение многих молекул с помощью метода валентных связей нельзя изобразить только одной валентной схемой с точной локализацией кратной связи, поскольку истинные свойства молекулы оказываются промежуточными между теми, которые отражаются в каждой отдельной схеме. [42]
Строение и свойства комплексных соединений объясняются координационной теорией, основы которой были заложены швейцарским химиком А. [43]
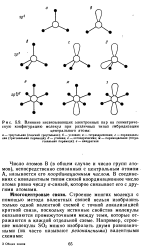 |
Влияние несвязывающих электронных пар на геометрическую конфигурацию молекул при различных типах гибридизации. [44] |
Строение многих молекул с помощью метода валентных связей нельзя изобразить только одной валентной схемой с точной локализацией кратной связи, поскольку истинные свойства молекулы оказываются промежуточными между теми, которые отражаются в каждой отдельной схеме. [45]
Страницы: 1 2 3 4