Современная теория - строение - атом
Cтраница 2
В основе современной теории строения атома лежит представление о двойственной природе м: икрочастиц, и в частности электронов. Оказывается, электроны могут вести себя и как частицы, и как волны - электроны обладают одновременно и корпускулярными и волновыми свойствами. [16]
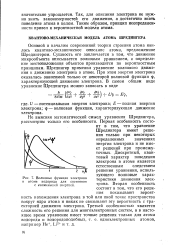 |
Волновые функции электрона. [17] |
Основой и началом современной теории строения атома явилось квантово-механическое описание атома, предложенное Шредингером. Сущность его заключается в том, что движение микрообъекта описывается волновым уравнением, а определение местоположения объектов производится по вероятностным принципам. [18]
Бора, Шредингера и других создателей современной теории строения атома и химической связи описаны в гл. Здесь мы совершим путешествие в более далекое прошлое и сосредоточим внимание на двух ученых, революционизировавших химию: один из них, Антуан Лавуазье ( 1743 - 1794), продемонстрировал, что важнейшим свойством, сохраняющимся в любой химической реакции, является масса, а другой, Джон Дальтон ( 1766 - 1844), выдвинул предположение об атомах как об элементарных частицах, участвующих в химических реакциях. В принципе Дальтон не первым выдвинул предположение об атомах, но он первым убедительно показал, что атомы действительно существуют и что они создают удобную основу для понимания химических реакций. [19]
Как впервые показал Бор, работы которого лежат в основе современной теории строения атома, движение электрона вокруг ядра квантуется. Точное описание атома требует применения волновой механики. Однако общим приемом при описании атомных систем является рассмотрение, в первую очередь, движения электрона на основании классической механики, а затем уже вопроса о том, какие изменения вносит в это движение квантовая теория. Этот метод неоднократно применялся в гл. IV и будет применен также при обсуждении атома водорода. Использование классических представлений не только дает основу для дальнейшего обсуждения и установления удобной номенклатуры, но для многих целей является также достаточно хорошим приближением. Поэтому классическая трактовка излагается весьма подробно, после чего рассматривается квантование движения и, наконец, излагаются некоторые соображения, связанные с волновой теорией. [20]
Истинная оценка споров была дана позже с позиций диалектического материализма и на основе современной теории строения атома. [21]
Представление об этих полях дает ясное объяснение характера межмолекулярных сил, первоначально возникшее на чисто физической основе за десятки лет до создания современных теорий строения атома и молекулы. [22]
Изучение внутреннего строения металлов и сплавов позволило утеным сделать вывод о том, что изменения свойств металлов и сплавов определяются особенностями их внутреннего строения. По современной теории строения атомов каждый атом состоит из положительно заряженного ядра и вращающихся вокруг него с огромной скоростью отрицательно заряженных электронов. [23]
Прежде всего было обращено внимание на то обстоятельство, что при окислении всегда увеличивается положительная валентность того или иного атома окисляемого вещества, а при восстановлении эта валентность уменьшается. Но с точки зрения современной теории строения атома изменение валентности элемента зависит от изменения числа электронов во внешней электронной оболочке атомов. Стало быть, при окислении валентность окисляемого элемента повышается за счет отдачи электронов. [24]
Спектральный анализ был открыт более 100 лет тому назад ( I860 г.) Кирхгофом и Бунзеном. Теория спектров легла в основу современной теории строения атома. Методы и задачи спектрального анализа, с одной стороны, и анализа спектров - с другой, существенно различны. Однако при рассмотрении спектрального анализа необходимо знать основные положения теории спектров. [25]
В этом ряду сделано исключение только для калия, который должен был бы стоять впереди аргона. Как увидим впоследствии, это исключение находит полное оправдание в современной теории строения атома. [26]
В этом ряду сделано исключение только для калия, который должен был бы стоять впереди аргона. Как увидим впоследствии, это исключение находит полное, оправдание в современной теории строения атома. [27]
Теория химического строения, созданная А. М. Бутлеровым ( I860 г), и развитая его учениками В. В. Марковниковым, А. М. Зайцевым и др., впервые дала руководящие идеи для оформления органической химии как науки. Эта теория основана на таких представлениях, как пространственное расположение атомов в составе молекулы, взаимное влияние атомов, входящих в состав одной молекулы, зависящее от их взаимного расположения, изомерия и элементы стереохимии. Это нашло подтверждение и уточнение в современной теории строения атома и теории химической связи, одинаково необходимой как в неорганической, так и в органической химии. [28]
Теория химического строения, созданная А. М. Бутлеровым ( 1860) и развитая его учениками В. В. Марковниковым, А. М. Зайцевым и др., способствовала оформлению органической химии как науки. Эта теория основана на таких представлениях, как пространственное расположение атомов в молекуле, взаимное влияние атомов, зависящее от их расположения, изомерия и элементы стереохимии. Это нашло подтверждение и уточнение в современной теории строения атома и теории химической связи, одинаково необходимой как в неорганической, так и в органической химии. [29]
В 1925 - 1926 гг. Гейзенберг ( Германия) и Шредингер ( Австрия) предложили независимо друг от друга два варианта новой механики; впоследствии было показано, что оба варианта приводят к тождественным результатам. Метод Шредингера оказался более удобным для выполнения расчетов; современная теория строения атомов и молекул основывается на этом методе. [30]
Страницы: 1 2 3