Теплоемкость - продукт
Cтраница 3
Воспользовавшись этим правилом, найдем теплоемкость продуктов взрыва гликольдинитрата С2Н4КзОб, образующего при взрыве продукты, состоящие из 14 грамм-атомов на грамм-молекулу ВВ. [31]
При содержании в твердом топливе влаги теплоемкость продуктов горения в интересующем нас температурном интервале, например от 0 до 2100, несколько выше вследствие того, что объемная теплоемкость водяного пара превышает среднюю объемную теплоемкость продуктов сгорания топлива в воздухе, содержащих высокий процент азота, обладающего низкой объемной теплоемкостью. [32]
Расчеты произведены с учетом изменения объемов и теплоемкостей реагирующих продуктов, теплопотерь в окружающую среду и пр. [33]
АСР и АС о представляют собой разности теплоемкостей продуктов реакции и реагирующих веществ при постоянном давлении и объеме соответственно. Отсюда очевидна основная трудность, возникающая при использовании ЛЯ для расчета зависимости констант устойчивости от температуры. С одной стороны, для точного определения углового коэффициента зависимости In К от 1 / Т желательно проводить исследования в как можно более широком интервале температур, но, с другой стороны, диапазон используемых температур ограничен температурной зависимостью АН. Проведение исследования в интервале температур порядка 30 С является обычным компромиссным решением. Если воспроизводимость используемого метода определения константы устойчивости составляет 3 %, то точность получаемого в конечном счете значения АН составляет примерно 0 85 кДж / моль, или 0 20 ккал / моль. [34]
На - падение теплосодержания теплоносителя; с - теплоемкость продукта; Ятп - теплопотери тепловой рубашки; tnK и и tnH - конечная и начальная температуры продукта; К - коэффициент теплопередачи от теплоносителя к продукту; F - ловерхность ТП; At - средняя логарифмическая разность температур. [35]
Таким образом, если теплоемкость исходных веществ больше теплоемкости продуктов реакции, то с повышением температуры выделение тепла при реакции возрастает. Как правило, именно это и наблюдается для образования соединений в области не слишком высоких температур. Значительно реже встречается противоположный случай: теплоемкость продуктов реакции оказывается больше теплоемкости исходных веществ; тогда тепловой эффект реакции при повышенной температуре меньше, чем при низкой. [36]
Количественная сторона этого положения легко уясняется из подсчетов теплоемкостей продуктов горения смешанного городского газа. Теплоемкости продуктов горения этого газа, приведенные в табл. 42, укладываются, как и следовало ожидать, в интервале между теплоемкостями доменного и природного газов. [37]
Температура пламени топлива вычисляется по его теплотворной способности и теплоемкости продуктов горения. При этом вводят некоторые допущения, которые упрощают расчет, но делают его не вполне точным. При расчетах исходят из следующих допущений: 1) горение происходит мгновенно и полностью; 2) состав и количество продуктов горения соответствуют стехиометрическим расчетам; 3) нет потерь тепла; 4) двуокись углерода и вода не диссоциируют. [38]
Для проверки точности этого положения применительно к газообразному топливу подсчитаны теплоемкости продуктов горения двух видов газообразного топлива, резко отличающихся по своему составу и по количеству необходимого для горения воздуха, а именно доменного газа и природного газа. [39]
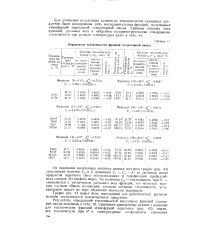 |
I Определение теплоемкостей фракций генераторной смолы. [40] |
График рис. 43 может быть использован для практических расчетов величин теплоемкостей рассмотренных продуктов. [41]
ДСр ( 2Ср) прод - ( 2Ср) реаг - разность теплоемкостей продуктов и реагентов. [42]
Обозначим через 2сн сумму теплоемкостей начальных ведомств и через 2ск - сумму теплоемкостей продуктов реакции. [43]
С; ( - начальная т-ра, С; С - разность теплоемкостей продуктов горения и компонентов исходной смеси; ДЯ ГОр - энтальпия сгорания. [44]
Закон, согласно которому температурный коэффициент теплового эффекта химической реакции равен разности сумм теплоемкостей продуктов реакции и исходных веществ. [45]
Страницы: 1 2 3 4