Упрочнение - связь
Cтраница 4
Полярность связи Si-О и экранирующее действие атомов кремния способствуют3 также упрочнению связи Si-С, которая по термостабильности превосходит связь С-С. [46]
На рис. 172 и 173 не видно оправдания тезиса Полинга об упрочнении связи при возрастании разности электроотрицательностей: в молекуле BF присутствует тройная связь, так же как и в молекуле N 2, но молекула BF, несмотря на возросшую разность электроотрицательностей, имеет менее прочную связь. Сравнение BF с N2 подробнее изложено в XII главе 1-го тома, где представлена вся сложность современного понимания связей в изоэлектронном ряду N 2, СО, BF. [47]
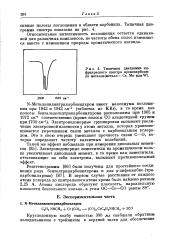 |
Типичная диаграмма инфракрасного спектра аренокарбони-ла металла ( металл - Сг, Мо или W. [48] |
Электронедонорные группировки вызывают увеличение электронной плотности у атома металла, которая уравновешивается упрочнением связи металла с карбонильным углеродом. Это в свою очередь уменьшает прочность связи С-О, которая определяет частоту валентных колебаний. [49]
Смещение частоты Р, к более высоким частотам может свидетельствовать о некотором упрочнении связи Р - С при комплексообра-зовании. В комплексе с переход - ным металлом эта пара электронов участвует в образовании связи никель-фосфор, и ее разрыхляющее влияние на связь Р - С становится меньше. [50]
Эти модели приведены на рис. 6.5 и 6.6. Мостиковая прокладка из галогенида способствует упрочнению связи металл - поверхность. Наиболее четко это выражено в случае иодида. Изображенная на рис. 6.6, а схема адсорбции может быть использована при моделировании многих других приэлектродных процессов и объяснении роли примесных ионов при электрокристаллизации металлов. Перенос заряда происходит с поверхности электрода, моделированного как кластер Си9, на частично дегидратированный комплекс в слое Гельмгольца. Расстояние между центрами соседних атомов составляет 250 пм. Мостик находится на равных расстояниях ( также 250 пм) от поверхности и от частично дегидратированного комплекса. [51]
Это влияние приводит к увеличению электронной плотности на фосфорильном кислороде и, следовательно, упрочнению связи Р - О-Ме. Из рис. 2 видно, что до CH ЗМ происходит ионообменная сорбция Меа с вытеснением Н из ZrP. В интервале 3 - 5 М НСЮ4 Kj практически не изменяется, т.е. сорбция происходит за счет взаимодействия сольвата металла с Р-0-группой сорбента. [52]
Смещение частоты v ( 4, к более высоким частотам может свидетельствовать о некотором упрочнении связи Р - С при комплексооб ра-зовании. Возможно это объясняется тем, что неподеленная пара электронов у атома трехвалентного фосфора в триалкилфосфинах оказывает разрыхляющее действие на связь Р - С. В комплексе с переходным: металлом эта пара электронов участвует в образовании связи никель-фосфор, и ее разрыхляющее влияние на связь Р - С становится меньше. [53]
Взаимодействие хемосорбированного радикала, находящегося в состоянии слабой связи, с кристаллом может привести к упрочнению связи. [54]
При переходе от одинарной связи к кратной межъядерные расстояния сокращаются, что можно связать с упрочнением связи. [55]
Из-за наличия М - эффекта в арилгалогенидах наблюдается сравнительная трудность замещения атомов галогенов, обусловленная упрочнением связи Ar-Hal. Несмотря на небольшое значение, М - эффект галогенов оказывает решающее влияние на направление вхождения заместителя при реакциях электрофильного замещения. [56]
Из-за наличия Л1 - эффекта в арилгалогенидах наблюдается сравнительная трудность замещения атомов галогенов, обусловленная упрочнением связи Аг-Hal. Несмотря на небольшое значение, М - эффект галогенов оказывает решающее влияние на направление вхождения заместителя при реакциях электрофильного замещения. [57]
Плотность и прочность пород, образующихся на умеренных глубинах, существенно зависит от соотношения между скоростью упрочнения межчастичных связей скелета и скоростью роста внешнего давления. [58]
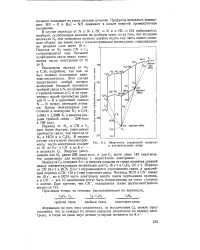 |
Энергетика соединений водорода и изоэлектронные ряды. [59] |
Переход от CN ( 9 е -) к HCN ( 10 е -) сопровождается упрочнением связи, а дальнейший переход к CN - ( 10 е -) еще упрочняет связь. Частицы HCN и CN - имеют по 10 е -, но в HCN часть электронов занята полем притяжения протона, а в CN - - все 10 электронов могут быть использованы на связь углерода с азотом. Еще прочнее, чем CN -, оказывается также десятиэлектронная молекула СО. [60]
Страницы: 1 2 3 4