Характер - изменение - потенциал
Cтраница 4
Оказалось, что характер изменения потенциала в зависимости от количества добавленной при титровании щелочи в точности соответствует изменению потенциала - с водородным электродом. [46]
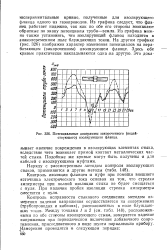 |
Потенциальные диаграммы закороченного ( недействующего. изолирующего фланца. [47] |
Из графика следует, что фланец работает надежно, так мак по обе его стороны возникают обратные по знаку потенциалы труба-земля. Из графика можно также установить, что изолирующий фланец находится в знакопеременном поле блуждающих токов. На другом графике ( рис. 326) изображен характер изменения потенциалов на неработающем ( закороченном) изолирующем фла.нце. Здесь обе кривые практически накладываются одна иа другую. [48]
Приемник вместе с источником питания смонтирован в отдельном металлическом корпусе и представляет собой избирательный усилитель с высокоомным входом. В приемнике имеется звуковая и визуальная индикация принимаемого сигнала. Принцип работы аппаратуры при определении мест повреждения изоляции сбстоит в регистрации характера изменений потенциалов вдоль газопровода. Потенциалы образуются при прохождении переменного тока частотой около 1000 Гц от генератора по цепи: генератор - газопровод - земля - генератор. Определение трассы газопровода и глубины его заложения основано на индуктивном методе. [49]
При диагностировании бурового оборудования электропараметрический метод служит основным методом контроля коррозии обсадных труб. Степень коррозии при этом оценивается косвенным методом по величине продольного электрического сопротивления трубы, измеряемого с помощью контактного зонда, опускаемого в скважину. В практике диагностирования подземных трубопроводов применяется аппаратура бесшурфового нахождения повреждения изоляции ( АНПИ), работа которой основана на регистрации характера изменения потенциалов вдоль трассы трубопровода. [50]
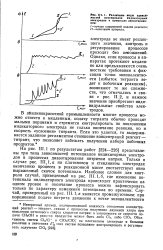 |
Различные виды зависимостей потенциалов индикаторных электродов в процессах диазотирова-ния. [51] |
I, а на платиновом и стеклянном электродах окончанию процесса в реакционной массе соответствует явно выраженный скачок потенциала. Наиболее сложен для контроля случай, приведенный на рис. 111.1 6, где изменение потенциала индикаторного электрода происходит практически на одном уровне и окончание процесса можно зафиксировать только по характеру изменения потенциала во времени. [52]
ОВ находится на низких и средних стадиях катагенеза, недостаточного для генерации УВ. В этих интервалах АВПД не наблюдается. Зона АВПД в бассейне Бохайс-кого залива в основном совпадает с главной зоной генерации углеводородов. Выше этой глубины в зоне гидростатических давлений характер изменения генерационного потенциала нефтема-теринских пород имеет вид пологой кривой с практически постоянным наклоном. Из рис. 1 видно наличие четкой связи между зоной АВПД и зоной генерации углеводородов в палеогеновых отложениях нефтегазоносного бассейна Бохайского залива. [53]
Однако реализовать кислородный электрод, поведение которого описывалось бы выведенными уравнениями, на практике весьма трудно. Это обусловлено особенностями, отличающими все газовые электроды и, кроме того, способностью кислорода ( особенно во влажной атмосфере) окислять металлы. На основную электродную реакцию накладывается поэтому реакция, отвечающая металлокис-ному электроду второго рода. Даже на платине могут образовываться окисные пленки, и поведение кислородного электрода не будет отвечать теоретическим уравнениям; эти отклонения проявляются, например, в характере изменения потенциала с давлением кислорода. Кроме того, имеются основания полагать, что реакция на кислородном электроде даже в отсутствие поверхностных окислов отличается от той, на которой основан вывод уравнения для потенциала кислородного электрода. [54]
Однако реализовать кислородный электрод, поведение которого описывалось бы выведенными уравнениями, на практике весьма трудно. Это обусловлено особенностями, отличающими все газовые электроды, и, кроме того, способностью кислорода ( особенно во влажной атмосфере) окислять металлы. На основную электродную реакцию накладывается поэтому реакция, отвечающая метал-локсидному электроду второго рода. Даже на платине могут образовываться оксидные пленки, и поведение кислородного электрода не будет отвечать теоретическим уравнениям; эти отклонения проявляются, например, в характере изменения потенциала с давлением кислорода. Кроме того, имеются основания полагать, что реакция на кислородном электроде даже в отсутствие поверхностных оксидов отличается от той, на которой основан вывод уравнения для потенциала кислородного электрода. [55]
Однако реализовать кислородный электрод, поведение которого описывалось бы выведенными уравнениями, на практике весьма трудно. Это обусловлено особенностями, отличающими все газовые электроды, и, кроме того, способностью кислорода ( особенно во влажной атмосфере) окислять металлы. На основную электродную реакцию накладывается поэтому реакция, отвечающая метал-локсидному электроду второго рода. Далее на платине могут образовываться оксидные пленки, и поведение кислородного электрода не будет отвечать теоретическим уравнениям; эти отклонения проявляются, например, в характере изменения потенциала с давлением кислорода. Кроме того, имеются основания полагать, что реакция на кислородном электроде даже в отсутствие поверхностных оксидов отличается от той, на которой основан вывод уравнения для потенциала кислородного электрода. [56]
Однако до сих пор не удалось практически реализовать кислородный электрод, поведение которого описывалось бы выведенными уравнениями. Это обусловлено особенностями, отличающими все газовые электроды и, кроме того, способностью кислорода ( особенно во влажной атмосфере) окислять все металлы. На основную реакцию накладывается поэтому реакция, отвечающая металлокисному электроду второго рода. Даже на платине могут образовываться окисные пленки и тогда поведение кислородного электрода не будет отвечать теоретическим уравнениям. Эти отклонения проявляются, например, в характере изменения потенциала с давлением кислородного газа. Кроме того, имеются основания полагать, что реакция на кислородном электроде, даже в отсутствие поверхностных окислов, отличается от той, на которой основан вывод уравнения для потенциала кислородного электрода. [57]
Однако практически реализовать кислородный электрод, поведение которого описывалось бы выведенными уравнениями, весьма трудно. Это обусловлено особенностями, отличающими все газовые электроды и, кроме того, способностью кислорода ( особенно во влажной атмосфере) окислять металлы. На основную электродную реакцию накладывается поэтому реакция, отвечающая металло-окисному электроду второго рода. Даже на платине могут образовываться окисные пленки и тогда поведение кислородного электрода не будет отвечать теоретическим уравнениям. Эти отклонения проявляются, например, в характере изменения потенциала с давлением кислорода. Кроме того, имеются основания полагать, что реакция на кислородном электроде даже в отсутствие поверхностных окислов отличается от той, на которой основан вывод уравнения для потенциала кислородного электрода. [58]
Страницы: 1 2 3 4