Число - неспаренный электрон
Cтраница 3
 |
Слоистая структура графита. Расстояние между слоями в 2 5 раза больше, чем между атомами в слоях. [31] |
АО, а число неспаренных электронов становится равным четырем. [32]
В ряде случаев число неспаренных электронов увеличивается в результате возбуждения атома, при котором двухэлектронные облака распадаются на одноэлектрон-ные. [33]
 |
Внутренние ( спаренные спины ( а и внешние ( свободные спины ( б. [34] |
Такое описание объясняет число неспаренных электронов, но при этом вводится довольно искусственное разделение комплексов на внутренние и внешние, предполагающие существенное различие в образовании связей. Этого удается избежать при использО Вании теории поля лигандов. [35]
В ряде случаев число неспаренных электронов увеличивается в результате возбуждения атома, при котором двухэлектронные облака распадаются на одноэлектронные. [36]
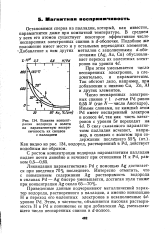 |
Влияние концентрации водорода и золота на парамагнитную восприимчивость их сплавов с палладием. [37] |
При этом уменьшается число неспаренных электронов, а следовательно, и парамагнетизм. Так обстоит дело, например, при добавлении к никелю Си, Zn, A. [38]
Во многих случаях число неспаренных электронов в атоме оказывается меньшим числа образованных им связей. Это объясняется тем, что при возбуждении атома происходит распаривание одной или нескольких внешних электронных пар с последующим переходом одного электрона от каждой пары на свободную и энергетически доступную ор-биталь более высокого подуровня. Для атома серы кроме основного состояния ( 2) возможны два возбужденных S ( 4 f) и S ( 6) за счет перехода соответственно одного или двух электронов на Зй-орбитали. [39]
Как видно, число неспаренных электронов в основном состоянии атомов не находится в согласии со значениями валентностей, отвечающими положению эле ментов в периодической системе. [40]
Полинг, увеличение числа неспаренных электронов от калия до хрома обусловливает постепенное возрастание механической прочности ( твердости) металлов, так как S -, р - и d - электроны принимают участие в образовании связей между атомами металла в его кристаллической решетке. После хрома в том же ряду элементов наблюдается понижение твердости. В химических связях с другими элементами переходные металлы очень часто используют два s - электрона, почему степень окисления 2 является для них важнейшей. [41]
 |
Окраска некоторых комплексных соединений кобальта. [42] |
Магнитные свойства определяются числом неспаренных электронов в комплексных соединениях. Например, в комплексе [ СоРб ] в образовании связей не участвуют Srf-электроны, поэтому четыре Зс. Комплекс [ СоРб ] 3 - высокоспиновый и парамагнитный. Поэтому этот комплекс ( гибридизация ( fsp3) - диамагнитен. [43]
Обычно валентность определяется числом неспаренных электронов на внешнем валентном электронном уровне. [44]
В круглых скобках указано число неспаренных электронов, рассчитанных из измерений магнитной восприимчивости. Другие смешанные циклобутадиеновые комплексы приведены в гл. [45]
Страницы: 1 2 3 4