Эндотермичность
Cтраница 2
Вследствие эндотермичности процесса диссоциации константа равновесия возрастает с увеличением температуры, но даже при 3000 и обычном давлении все еще не заметна диссоциация. Большая прочность связи NN в молекуле азота объясняет в принципе его химическую инертность, а также то, что большинство простых соединений азота эндотермичны, даже если они имеют прочные связи. Объясняется это тем, что N2, во-первых, совершенно не-полярен и, во-вторых, обладает значительно более высоким потенциалом ионизации, чем все перечисленные системы. Так, известно, что как - СС -, так и - СМ-группы могут быть донорами за счет своих я-электронов, а: СО: за счет неподеленной пары электронов атома углерода. [16]
Вследствие эндотермичности процесса диссоциации константа равновесия возрастает с увеличением температуры, но даже при 3000 и обычном давлении все еще не заметна диссоциация. Большая прочность связи NN в молекуле азота объясняет в принципе его химическую инертность, а также то, что большинство простых соединений азота эндотермичны, даже если они имеют прочные связи. Объясняется это тем, что N2, во-первых, совершенно не-полярен и, во-вторых, обладает значительно более высоким потенциалом ионизации, чем все перечисленные системы. Так, известно, что как - СС -, так и - СН-группы могут быть донорами за счет своих п-электронов, а: СО: за счет неподеленной пары электронов атома углерода. [17]
Вследствие эндотермичности процесса термодеструкции а-полиоксиметилена и параформальдегида и низкой теплопроводности СН2О выделяющийся мономер имеет сравнительно невысокую температуру. Это весьма существенно, так как при повышенных температурах формальдегид легко вступает в реакции, которые катализируются металлическими стенками аппаратов и снопообразными продуктами, образующимися при пиролизе. В лабораторных установках время поебывания мономерного формальдегида в зоне высоких температур невелико, что приводит к снижению количества образующихся побочных продуктов. [18]
Уменьшение эндотермичности процесса диссоциации, которое метет быть вызвано варьированием структуры образующегося катиона, уходящей группы или изменением природы растворителя, должно приводить к сдвигу переходного состояния в сторону исходного, т.е. к уменьшении степени разрыва связи с уходящей группой в переходном состоянии и к уменьшению разделения зарядов в нем. [19]
Благодаря этой эндотермичности обратные реакции протекают быстро и их вклад оказывается заметным даже при образовании небольших количеств продукта. [20]
 |
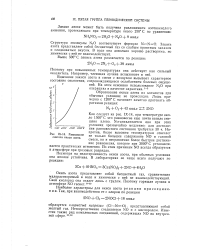
Равновесие весне еще почти нацело смещено влево. Уста-синтеза нитроксида. навливается оно при этих условиях чрезвычайно медленно. для достижения равновесного. [21] |
Несмотря на эндотермичность, оксид азота при обычных условиях вполне устойчив. [22]
Легкость ( низкая эндотермичность) распада ионов с отщеплением третичных карбкатионов приводит к накоплению изоструктур в продуктах распада алканов, содержащих 7 и более атомов углерода. [23]
Несмотря на эндотермичность окиси азота, при обычных условиях она вполне устойчива. [25]
Таким образом, эндотермичность ( AU) предполагает наличие активационного барьера для процесса. [26]
Дегидрирование углеводородов вследствие эндотермичности процессов требует интенсивного подвода тепла. Это в значительной степени и определяет их технологическое оформление. Так, в циклических процессах применяют твердый инертный разбавитель-теплоноситель. Использование такого теплоносителя позволяет аккумулировать тепло, выделяющееся при регенерации катализатора, и затем использовать его при дегидрировании. При дегидрировании олефиновых и алкилароматических углеводородов в качестве теплоподводящего агента используют водяной пар. [27]
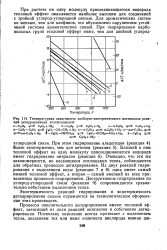 |
Температурная зависимость изобарно-изотермического потенциала реакций дегидрирования углеводородов. [28] |
Экзотермичность реакций гидрирования и эндотермичность дегидрирования сильно отражаются на технологическом оформлении этих производств. [29]
Все окислы хлора характеризуются эндотермичностью процессов их образования из простых тел. [30]
Страницы: 1 2 3 4