Гексаммин
Cтраница 3
Из полученного водного раствора NiCl2 никель выделяют получением его хлористого гексаммина Ni ( NH3) eCl2, который после обработки окисью углерода при 170 С и 200 am снова образует тетракарбонил никеля. [31]
Вновь полученные данные в сочетании с ранее установленным отсутствием образования гексаммина при замене этиламинового производного на аммиачную соль Гро привели нас к выводу, что образование гексаммина при реакции Гринберга и Гильдеигершеля связано с окислительно-восстановительными превращениями. [32]
Введение в реакционную среду KMn04, MnS04 или Н202 препятствует образованию гексаммина. [33]
При обработке раствора водным аммиаком получаются два аммиаката, а именно: гексаммин Ni ( Re04) 2 6NH3, выделяющийся в виде сиреневых кристаллов, и тетрам-мин Ni ( Re04) 2 4NH3, бледноголубое вещество, остающееся в растворе. При нагревании эти аммиакаты разлагаются с образованием окиси никеля. [34]
Введение в реакционную среду молекулярного хлора ( также гипо-хлорита) дает возможность получить гексаммин из разнообразных производных двух - и четырехвалентной платины. Этот способ ведения реакции, не будучи приспособленным для использования в качестве метода получения гексаммина, представляет интерес для вскрытия механизма его образования. Механизм этот состоит в многократном попеременном восстановлении и окислении платины, сопровождающимися переходом от октаэдрической конфигурации к плоскостной и обратно. [35]
Попеременное восстановление и окисление, происходящие в изучаемой нами системе, принципиально аналогичны условиям синтеза гексаммина по Дрекселю-Гердесу. [36]
Соль выпадает в виде желтоватых гексагональных табличек или октаэдров при действии йодистого калия на растворы других гексамминов родия. При нагревании, начиная с 185 С, замечается разложение соли, ло продукты разложения не исследованы. [37]
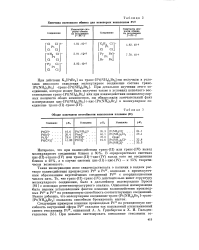 |
Кинетика изотопного обмена для некоторых комплексов Ft11.| Общие константы нестойкости комплексов платины ( II. [38] |
Следующим примером влияния производных Pt11 на реакционную способность внутренней сферы PtIV оказался так называемый алкиламиновый синтез гексаммина PtIV, описанный А. А. Гринбергом и X. [39]
После этого смесь промывали большим количеством холодной воды, в которой нитратопентаммин значительно труднее растворим, чем гексаммин. Фильтрат представляет собой очень разбавленный раствор гексаммина, который осаждали пирофосфатом натрия. Соль представляет собой белый кристаллический порошок, мало растворимый в воде, нерастворимый в разбавленной азотной кислоте. Кристаллы имеют форму пирамид или тонких игл. Будучи нагреты в токе водорода, взрывают. SiFe ] 2 -, [ PtCleP -, [ AuClJ -, [ Fe ( CN) e ] 4, [ Fe ( CN) e ] 3 - дают с нитратом гексаммина характерные осадки. [40]
Затем раствор нейтрализуют разбавленной соляной кислотой, охлаждают его и отфильтровывают на воронке Бюхнера уголь и кристаллы гексаммина. Смесь на фильтре промывают теплой водой, содержащей несколько капель соляной кислоты. Фильтрат нагревают до 80 и добавляют концентрированной соляной кислоты, пока не появится стойкая муть. Все это медленно охлаждают, осадок гексаммина фильтруют и промывают спиртом. [41]
Соль выпадает в виде блестящих снежно-белых гексагональных призм или ромбических табличек даже из очень разбавленных нейтральных растворов солей гексаммина при добавлении пирофосфата натрия. В вакууме при обыкновенной температуре вещество теряет 20 молекул воды, а остальные три молекулы отщепляются только при нагревании. [42]
Основные соли кобальта, а также гидрозакись его легко растворяются в избытке аммиака и аммонийных солей с образованием нестойкого гексаммина кобальта [ Со ( МН3) б ] С12 грязно-желтого цвета. [43]
Наиболее важное исключение встречается в случае бромида и йодида кадмия, где не существует никаких промежуточных соединений между гексаммином и диаммином, а также в случае галогенидов меди ( II), где устойчивыми промежуточными соединениями являются вместе тетраммина аммиакаты с З / г молекулы аммиака на атом меди. [44]
Приведенные данные показывают, что колебание содержания аммиака в пределах 10 - 5 мл почти не отражается на составе и выходе гексаммина. Дальнейшее уменьшение содержания аммиака сопровождается как уменьшением выхода, так и ( в случае 1 мл NH4OH) изменением состава твердой фазы. При отсутствии аммиака образующийся продукт в основе, по-видимому, представляет собой хлорид Гро, содержащий примесь соединений с меньшим содержанием хлора. [45]
Страницы: 1 2 3 4