Гидрид - церие
Cтраница 2
Из растворов солей тяжелых металлов гидрид церия осаждает металл; с азотнокислыми и хлорнокислыми солями дает взрывчатые смеси. [16]
Велером в 1857 г. [12], а гидриды церия, тория [13] и циркония [14] были получены Винклером в 1891 г. Гидрид лития найден Хрустом [15] и Муассаном [16] в результате изучения системы литий - водород. [17]
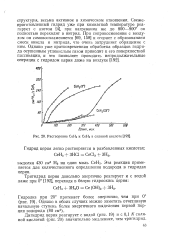 |
Растворение СеН2 и СеНз в соляной кислоте. [18] |
Эта реакция применяется для количественного определения водорода в гидридах церия. [19]
Несмотря на то, что первые гидриды рзэ ( гидриды церия) были получены еще в начале этого столетия, достаточно полные сведения 5 их структуре и условиях образования появились лишь в последнем десятилетии. [20]
В работе М. Е. Кост и Г. А. Гольдера [185] измерена плотность образцов гидрида церия в интервале концентраций СеН0 2 - СеН3 аргоновым методом. [21]
 |
Установка для получения Се-3 алсИШрилиаим риспли. [22] |
Описанный метод получения труднодоступен, так как требует применения сложной аппаратуры с высоким вакуумом и использования гидрида церия, работа с которым крайне затруднительна из-за его пиро-форности. [23]
До недавнего времени в литературе была известна лишь одна работа Росси [165] с кратким сообщением о кристаллической структуре гидрида церия. Согласно этой работе, гидрид церия имеет кубическую гранецентрированную решетку со стороной элементарного куба ао 5 61 А. Откачивание водорода при 530 приводит к появлению второй фазы с несколько меньшим периодом решетки. [24]
Редкоземельные металлы взаимодействуют с водородом медленно при комнатной температуре, быстрее - при более высоких температурах ( 250 - 300) При этом образуются гидрид церия в виде красно-коричневой массы, гидрид лантана в виде черной массы, гидриды неодима и празеодима в виде блестящей аморфной индиго-синей массы. [25]
 |
Изменение структуры полуторных окислов Р. м. в зависимости от темп-ры и порядкового номера элемента. А - гексагональная, В - тригональная ( ромбич. или моноклинная, С - кубическая. [26] |
Гидриды обладают различной термохи-мич. Гидрид церия при комнатной темп-ре реагирует с азотом, а при нагревании до 800 - 900 переходит в нитрид. На воздухе гидрид воспламеняется с образованием смеси окисла и нитрида. Для предотвращения подобного разрушения гидрида применяется его обработка осушенным углекислым газом. Рг и Nd при комнатной темп-ре инертны к водороду и только при 300 - 400 активно его абсорбируют. [27]
По химическим свойствам гидриды РЗЭ существенно отличаются друг от друга. Гидрид церия самовоспламеняется на воздухе. Гидриды РЗЭ неустойчивы во влажном воздухе - превращаются в гидроокиси или карбонаты. [28]
Цериевые металлы и церий в том числе способны активно поглощать водорол. Гидрид церия был впервые получен нагреванием окиси его с магнием в атмосфере водорода. Состав водородистого соединения иерия был найден отвечающим формуле СеНз 1, а теплота образования определена ранной 56 750 ккал / г-атом. При нагревании в вакууме гидрид церия разлагается на металл и водород. [29]
 |
Изменение структуры полуторных окислов Р. м. в зависимости от темп-ры и порядкового номера элемента. А - гексагональная, В - тригональная ( ромбич. или моноклинная, С - кубическая. [30] |
Страницы: 1 2 3 4