Гидрирование - аллилового спирт
Cтраница 2
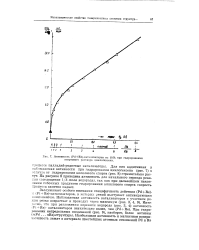 |
Активность ( Рс1 КЬ-катадизаторов на SiO2 при гидрировании спиртового раствора циклогексена. [16] |
Для них аддитивная и наблюдаемая активности при гидрировании циклогексена ( рис. 7) в отличие от гидрирования аллилового спирта ( рис. 8) стремительно растут. На рисунке 8 приведена активность для начального периода реак-шш ( поглощение 1 / 3 моля водорода), так как при дальнейшем накоплении побочных продуктов гидрирования аллилового спирта скорость процесса заметно падает. [17]
Изучена активность бинарных металлических ( Мед Мев) - адсорбционных катализаторов в реакциях разложения перекиси водорода, гидрирования аллилового спирта и циклогексена. Во взятых системах Me A - один из постоянных компонентов: палладий или платина, Me в - варьируемые компоненты: рутений, родий, осмий, иридий, рений и серебро. [18]
Последовательность изменения энергии связей металл-водород в ряду PdBPtBRhB находится в соответствии с изменением каталитической активности указанных металлов в реакции ясидкофазно-го гидрирования аллилового спирта. [19]
 |
Гидрирование аллилового спирта в воде на ( Pd nRe / BaCO3 катализаторах. 1 и 2 - наблюдаемая. активность. 3 и 4 - аддитивная активность. [20] |
Однокомпонентные рениевые катализаторы и в этом процессе оказались совершенно неактивными, вследствие чего аддитивная активность ( Pt wRe) - и ( Pd Re) - систем остается на уровне постоянного компонента. Таким образом, при гидрировании аллилового спирта имеет место четкий разрыв аддитивной и наблюдаемой активности. Наблюдаемая активность при концентрациях рения, соответствующих максимуму, в 5 - 6 раз превышает аддитивную. [21]
 |
Гидрирование аллило. [22] |
Однокомпонентные рениевые катализаторы и в этом процессе оказались совершенно неактивными, вследствие чего аддитивная активность ( Pt raRe) - и ( Pd Re) - систем остается на уровне постоянного компонента. Таким образом, при гидрировании аллилового спирта имеет место четкий разрыв аддитивной и наблюдаемой активности. Наблюдаемая активность при концентрациях рения, соответствующих максимуму, в 5 - 6 раз превышает аддитивную. [23]
Приведены результаты определения фазового состава, удельной поверхности и адсорбционной способности по отношению к водороду, метанолу и алли-ловому спирту боридных катализаторов, полученных из солей платины, палладия и родия. Измерена удельная активность катализаторов в реакции гидрирования аллилового спирта. [24]
Сравнение полученных экспериментальных данных с ранее проведенными исследованиями свойств платнио-репиевых и палладий-рение-вых катализаторов на сахарном угле и SiOg [1-3] показывают, что носитель оказывает влияние лишь на величину активности, при этом с изменением его природы возможно некоторое смещение положения максимума активности в пределах указанных атомных отношений. Величина наблюдаемой активности ( Pt Re) - и ( Pd nRe) - катализаторов при гидрировании аллилового спирта уменьшается в ряду носителей: SiO2 BaCO3сахарный уголь. [25]
Сравнение полученных экспериментальных данных с ранее проведенными исследованиями свойств платино-рениевых и палладий-рениевых катализаторов на сахарном угле и SiO2 [1-3] показывают, что носитель оказывает влияние лишь на величину активности, при этом с изменением его природы возможно некоторое смещение положения максимума активности в пределах указанных атомных отношений. Величина наблюдаемой активности ( Pt nRe) - и ( Pd rcRe) - катализа-торов при гидрировании аллилового спирта уменьшается в ряду носителей: 5Ю2л ВаСОзсахарный уголь. [26]
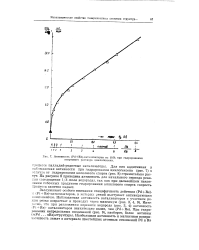 |
Активность ( Рс1 КЬ-катадизаторов на SiO2 при гидрировании спиртового раствора циклогексена. [27] |
Для них аддитивная и наблюдаемая активности при гидрировании циклогексена ( рис. 7) в отличие от гидрирования аллилового спирта ( рис. 8) стремительно растут. На рисунке 8 приведена активность для начального периода реак-шш ( поглощение 1 / 3 моля водорода), так как при дальнейшем накоплении побочных продуктов гидрирования аллилового спирта скорость процесса заметно падает. [28]
Энергия образования непредельных соединений, содержащих гидроксильный или эфирный кислород при ненасыщенном углеродном атоме, больше, чем энергия образования изомерных им соединений, в которых кислород находится при насыщенном углеродном атоме. Вывод о большей энергии образования этих соединений может быть сделан на основании сравнения теплот гидрирования этиленовой связи в углеводородах и кислородсодержащих соединениях указанного типа ( табл. 24, ср. В табл. 24 приведена теплота гидрирования аллилового спирта, в котором кислородный атом стоит при насыщенном углеродном атоме; теплота гидрирования его близка к теплоте гидрирования пропилена. [29]
Хроматографический анализ продуктов гидрирования пропаргилового спирта показал, что на Pd-черни в воде происходит изомеризация получающегося аллилового спирта в пропионовый альдегид ( до 31 %), причем пропи-оновый альдегид появляется в продуктах реакции с самого начала процесса. При модифицировании Pd-черни катионами кадмия удается подавить не только гидрирование аллилового спирта до пропи-лового, но и реакцию изомеризации аллилового спирта. [30]
Страницы: 1 2 3