Алкильный гомолог
Cтраница 2
 |
Бицикло ( 3 3 0 октан ( пенталан. [16] |
Молекула тряис-пенталана весьма напряжена и под влиянием соответствующих катализаторов полностью перегруппировывается в значительно более устойчивую г цс-форму. В нефтях встречаются лишь г цс-пенталан и его алкильные гомологи. Поэтому стереохимию бицикло ( 3 3 0) октана мы в дальнейшем будем рассматривать лишь для мс-соединений, опуская в целях простоты эту приставку. [17]
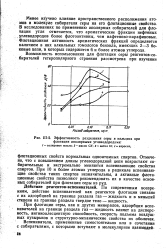 |
Эффективность разделения серы и кальцита при. [18] |
Менее изучено влияние пространственного расположения атомов в молекуле собирателя серы на его флотационные свойства. Флотационная активность ароматических фракций определяется наличием в них алкильных гомологов бензола, имеющих 2 - 3 боковые цепи, в которых содержится 6 и более атомов углерода. [19]
 |
Хроматограмма равновесной смеси ( 400 К бицикло ( 4 4 0 деканов состава С. 2. [20] |
На термодинамическую устойчивость трициклических насыщенных углеводородов большое влияние оказывает исключительно высокая устойчивость структуры адамантана, состоящего из трех кресловидных циклогексановых колец. Система связки колец в эдамантане лишена каких-либо напряжений, поэтому адамантан и его алкильные гомологи безусловно более устойчивы, чем любые изомерные им трициклитеские углеводороды. [21]
 |
Пространственные изомеры бицикло ( 4 3, Основана ( гидринцана. [22] |
Система бицикло ( 4 3 0) нонана ( гидриндана) является чрезвычайно важной для химии природных соединений. Достаточно здесь напомнить хорошо известную систему колец С и D в стероидах. В то же время стереохимия бицикло ( 4 3 0) нонана и его алкильных гомологов является весьма своеобразной и, без сомнения, самой сложной из всех бициклических систем, рассматриваемых в данной работе. [23]
Алкилирование арена повышает его основность и, следовательно, реакционную способность. Поэтому в лабораторных условиях обычно трудно остановить реакцию на нужной стадии алкилиро-вания. Так, из бензола, метилбромида и бромида алюминия образуется 1 2 4 5-тетраметилбензол, который более основен, чем низшие его алкильные гомологи, однако в дальнейшее алкилирова-ние это соединение вступает нелегко, так как оба свободных места в ядре блокированы соседними о-метильными группами, пространственно затрудняющими атаку электрофильного партнера. Для синтеза низших продуктов алкилирования следует выбирать мягкий катализатор Фриделя - Крафтса. [24]
Страницы: 1 2