Девиль
Cтраница 1
Девиль, Стае [5] и Джилкрист [5] предложили способ переведения в растворимое состояние металлического родия путем предварительного сплавления его со свинцом и серебром. [1]
Девиль [146] сообщает, что если сырой хлористый алюминий смешать с железными стружками и смесь расплавить под давлением, то хлорное железо восстанавливается в хлористое, которое является значительно менее летучим, чем хлорное железо. Таким образом возогнанпый хлористый алюминий содержит меньше железа и слабее окрашен. [2]
Девиль в процессе получения металла заменяет калий более дешевым натрием и проводит лабораторные опыты в крупном масштабе. Полученный хлорид алюминия загружался в большую стальную трубу, в которой на равном расстоянии друг от друга были расставлены сосуды, наполненные металлическим натрием. [3]
Девиля по диссоциации, как справедливо отметил Бекетов2, составляют не только историческую эпоху в развитии химии, но и поворот в направлении изучения химии. [4]
Когда Девиль делал доклад в Парижской академии наук, он даже не мог дать ответа, с какой глубины была взята кавказская нефть и из какого месторождения. [5]
Сент-Клер Девиль, работая над способом получения алюминия электролизом, вслед за Деви и Бунзеном [ Bunsen ] заметил, что глинозем хорошо растворяется в расплавленном криолите. [6]
Сент-Клер Девиль во Франции применил способ Велера для первого промышленного производства алюминия, внеся в него некоторые улучшения. В частности, Сент-Клер Девиль заменил применявшийся в качестве восстановителя калий более дешевым металлическим натрием, а затем очень гигроскопичный летучий хлористый алюминий-двойным хлоридом алюминия и натрия. Производство алюминия по этому так называемому химическому способу было организовано Сент-Клер Девилем в Жавей, под Парижем. В дальнейшем для получения алюминия при аомощи этого способа были построены небольшие заводы в Англии, США и Германии. В течение первых 10 лет после изобретения Сент-Клер Девиля в мире было произведено лишь 10 т алюминия. [7]
Еще Сен-Клер Девиль [2] наблюдал, что при нагревании ТЮ2 в присутствии НС1 обнаруживается рост кристаллов и окисел приобретает при этом голубой цвет. Очевидно, двуокись титана осаждается при транспорте по уравнению ( 114) с дефицитом кислорода. [8]
Еще Сен-Клер Девиль [2] наблюдал, что при нагревании Ti02 в присутствии НС1 обнаруживается рост кристаллов и окисел приобретает при этом голубой цвет. Очевидно, двуокись титана осаждается при транспорте по уравнению ( 114) с дефицитом кислорода. [9]
Эксперименты Сен-Клер Девиля были связаны с изучением процессов образования природных минералов. Однако трудно привести конкретные примеры из этой области, не прибегнув к различным гипотезам, поскольку существующие минералы представляют собой лишь конечные продукты процессов, для которых, как правило, отсутствуют какие-либо сведения об исходных веществах и их последующих превращениях. В общем очевидно, что происходящие в природе транспортные реакции являются реакциями особого типа, относящимися к весьма обширной области процессов пневматолитического минералообразования. [10]
По способу Сент-Клер Девиля с 1855 по 1890 год было получено всего 200 тонн алюминия; за оставшиеся до конца XIX века 10 лет его выплавка ( уже по новому способу) составила 28000 тонн, а в 1930 году мировое производство металла достигло 300000 тонн. [11]
Трудности опытов Сент-Клер Девиля были связаны с необходимостью быстрого охлаждения продуктов диссоциации и создания эффективного способа разделения их друг от друга. При этом устанавливается химическое равновесие, которым можно управлять, изменяя температуру и давление. [12]
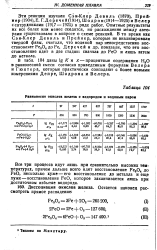 |
Равновесие окислов железа с водородом и водяным паром. [13] |
Эти реакции изучали Сэн-Клер Девиль ( 1870), Прей-нер ( 1904) Е. Г.Деречей ( 1914) Шодрон ( 1914 - 1925) иВелер с сотрудниками ( 1917 - 1925) в ряде работ. Опытные результаты их все более или менее сходятся, но расхождение между авторами существовало в вопросе о схеме реакций. В то время как Сэн-Клер Девиль иПрейнер, которые не анализировали твердой фазы, считали, что водяной пар непосредственно вос-становляет Fe3O4 до Fe, Деречей и др. показали, что это восстановление идет в две стадии: сначала до FeO и лишь затем до металла. [14]
Это было известно еще Сен-Клер Девилю и его ученикам. [15]
Страницы: 1 2 3 4