Деструкция - поливинилхлорид
Cтраница 2
Можно предположить, что продукты распада диметилформ-амида ( диметиламин) в процессе деструкции поливинилхлорида по радикальному механизму действуют двояко. С одной стороны, амин, присоединяя радикалы ROO - и образуя малоактивный радикал-комплекс, тормозит окисление. С другой стороны, в результате очень высокой чувствительности поливинилхлорида к азотсодержащим соединениям основного характера дегидрохлориро-вание полимера ускоряется. [16]
Обнаружение винилхлорида и его идентификация в подобных композициях загрязнителей ( например, в продуктах деструкции поливинилхлорида [424]) крайне затруднительна. Достоверная идентификация винилхлорида осложняется еще и тем, что его молекула чрезвычайно инертна. [17]
Разуваева, К. С. Минскера, Б. Б. Троицкого, В. С. Пу-дова внесен существенный вклад в выяснение кинетических закономерно-стей и механизма деструкции поливинилхлорида [117-119], что позволило значительно повысить стабильность этого важного в практическом отношении полимера. [18]
Значительное число работ в этом направлении252 - 264 наглядно показывает необходимость более детального выяснения некоторых аспектов механизма деструкции поливинилхлорида. [19]
Целью нашей работы было изучение некоторых особенностей ингибирующего действия стабилизаторов, которые различаются по своей способности связывать хлористый водород, отщепляющийся при деструкции поливинилхлорида. [20]
В присутствии значительных количеств кислорода процесс отщепления НС1 сильно ускоряется, причем образуются несшитые продукты деструкции. Исследование процессов деструкции поливинилхлорида методом ИК-спектроскопии в отсутствие и в1 присутствии кислорода показало, что в последнем - случае в полимере появляется значительное число карбонильных групп 307 - зо9 ( полоса 1730 см-1) -, образующихся при реакции кислорода с полимерными радикалами. [21]
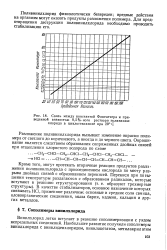 |
Связь между константой Фикентчера и приведенной вязкостью 0 5 % - ного раствора поливинил-хлорида в циклогексаноне при 20 С. [22] |
Поливинилхлорид физиологически безвреден; вредные действия на организм могут оказать продукты разложения полимера. Для предотвращения деструкции поливинилхлорида необходимо проводить стабилизацию его. [23]
В интервале температур от 200 до 250 С кинетика выделения хлористого водорода соответствует цепной реакции с вырожденными разветвлениями и энергией активации 33 ккал / моль. Авторы полагают, что деструкция поливинилхлорида происходит по радикальному механизму, причем в интервале температур от 150 до 190 С активными центрами являются в основном ненасыщенные аллильные группы на концах цепей полимера. При 200 - 250 С активными центрами могут служить разветвления цепи и другие места нарушения регулярности структуры полимера. Обрыв реакцион-ноепособяых цепей может происходить за счет взаимодействия макрорадикалов, что приводит к образованию межмолекулярных сшивок. [24]
При температурах переработки от 150 до 190 С происходит деструкция поливинилхлорида, сопровождающаяся выделением хлористого водорода и других побочных продуктов. Для предотвращения деструкции и снижения температуры переработки в ПВХ вводят стабилизаторы, антиоксиданты и пластификаторы. [25]
При окрашивании литьевых изделий следует учитывать, что вид и концентрация вводимого пигмента могут влиять на режим переработки материала. Для поддержания композиции в расплавленном состоянии при переработке приходится повышать температуру, а это может привести к деструкции поливинилхлорида и снижению эксплуатационных свойств изделий. В случае пигментирования поливинилхлорида органическими пигментами может иметь место гелеобразование и, как следствие, разогрев поливинилхлоридной массы, что также может вызвать деструкцию полимера. [26]
Деструкция некоторых полимеров сопровождается выделением веществ, которые ускоряют дальнейший процесс расщепления полимера. При деструкции поливинилхлорида выделяется хлористый водород, который действует автокаталитически на дальнейший процесс расщепления полимера. Замедлить деструкцию таких полимеров могут соединения, способные поглощать вещества, выделяющиеся из полимеров. [27]
Температура разложения является условной величиной при характеристике термостойкости полимеров. Она зависит от метода определения и продолжительности теплового воздействия. Например, деструкция поливинилхлорида может начаться при 180, 150 и даже 120 С в зависимости от длительности нагревания. [28]
Как отмечено рядом авторов, Оловоорганические соединения имеют ряд преимуществ по сравнению с другими стабилизаторами. В частности, они повышают термическую устойчивость и светостойкость полимера и являются антиоксидантами. Стабилизаторы, не содержащие олова, после выполнения своей функции часто ускоряют деструкцию поливинилхлорида. Следует отметить, что Оловоорганические соединения являются не только термо - и светостабилизаторами. [29]
Другие методы подбора термостабилизаторов, такие, как измерение скорости де-гидрохлорирования поливинилхлорида, менее надежны, чем две товой тест. К наиболее важному типу термостабилизаторов относятся соединения свинца, которые реагируют с выделяющимся при деструкции поливинилхлорида хлористым водородом, образуя хлорид свинца. Чаще всего, по-видимому, употребляется основной карбонат свинца. Однако его недостатком является способность выделять двуокись углерода, что может привести в некоторых условиях к вспениванию материала. Другие соединения свинца применяются лишь в специальных случаях. Так, средний фталат свинца служит стабилизатором в композициях, используемых для изготовления термостойкой электроизоляции и патефонных пластинок типа хай-фи. Помимо соединений свинца, которые-являются наиболее распространенными термостабилизаторами поливинилхлорида, все шире употребляются соли других металлов, в частности стеараты, каприлаты и пальмитаты цинка и кадмия. Еще одну группу термостабилизаторов составляют органические соединения олова, которые первоначально были использованы из-за того, что они дают прозрачные композиции. Однако самые первые представители этой группы, такие, как дикаприлат ди-бутилолова, не придавали поливинилхлориду достаточную тер мостойкость; поэтому в настоящее время они постепенно вытесняются другими оловоорганическими стабилизаторами, например малеатом дибутилолова. [30]
Страницы: 1 2 3