Константа - скорость - элементарная стадия
Cтраница 3
В общем случае константа скорости рекомбинации определяется соотношением l / k l / kn, где kn - константа скорости ге-й элементарной стадии. Уравнение кинетики при этом не всегда может быть представлено в виде dR / dt k ( T) f [ R ], что является необходимым условием для применения уравнения Аррениуса. [31]
Так же, как и в реакциях низкомолекулярных соединений, наибольшую сложность здесь представляет проблема выделения из эффективной скорости реакции констант скорости элементарных стадий. Далеко не всегда удается получить константы скорости роста полимерной цепи, в связи с чем количественная оценка роли растворителя в процессах полимеризации весьма затруднена. В некоторых случаях в процессах полимеризации при замене растворителя удается очень резко изменить скорость протекания реакции, причем иногда до изменения механизма реакции роста цепи. Укажем, в частности, на резкое изменение скорости ионной полимеризации в полярных и сильно сольватирующих противоион средах, когда рост цепи, осуществлявшийся на ионных парах или более сложных ассоциатах, под действием растворителя происходит уже на более активных в кинетическом отношении центрах - свободных ионах. При радикальной полимеризации известны случаи изменения констант скорости роста цепи на несколько порядков при введении в систему специальных добавок, образующих комплексы с мономером, способные к специфической координации с активным центром растущей цепи. Последнее явление чрезвычайно распространено также при ионно-координационной полимеризации. [32]
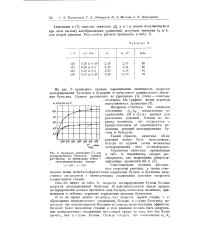 |
Проверка уравнения ( 7 для. [33] |
Сопоставление величин абсолютных скоростей реакции, а также отмеченных выше свойств поверхностных соединений бутана и бутилена качественно согласуется с вычисленными значениями констант скоростей элементарных стадий. [34]
Возможность появления множителей, приводящих к компенсационным эффектам, вероятно, следует искать в суммарных выражениях констант скорости, а ее в константах скоростей элементарных стадий. Так, трактовку [392] фактически можно рассматривать как предположение о протекании реакции на неоднородной поверхности катализатора с экспоненциальным распределением по теплотам адсорбции при наличии соотношения линейности. Тогда в выражении константы скорости может появиться множитель с энергией активации в экспоненте, не зависящим от температуры. [35]
В результате изменения значений параметров реакционной смеси нестационарными могут оказаться концентрации промежуточных образований каталитического цикла и состояния приповерхностного слоя катализатора, вызывающие изменения констант скорости элементарных стадий. Для достаточно быстрых реакций, представляющих практический интерес, масштаб времени изменения поверхностных концентраций Mf лежит большей частью в интервале 10 - - 102 с. При изменении свойств катализатора, связанных с изменением строения поверхности и состава приповерхностного слоя, приближение к стационарному состоянию обычно включает стадии, отличные от стадий каталитической реакции. Поэтому в большинстве случаев приближение к стационарному состоянию осуществляется намного медленнее протекания каталитической реакции. [36]
Таким образом, реакции с преобладанием перекрестного обрыва возможны, хотя и требуют довольно жесткого соотношения между концентрациями активных центров, а следовательно, между константами скоростей элементарных стадий продолжения цепи, в которых принимают участие эти активные центры. [37]
В области жидкофазного окисления основное содержание этого периода состоит в количественном изучении процессов, установлении новых реакций зарождения радикалов, разветвления и обрыва цепей, определении констант скоростей элементарных стадий, выявлении особенностей действия растворителей. [38]
Кинетика реакций окисления жидких олефинов очень подробно изучена Болландом [22] и Бейтманом [23], причем известно большое количество данных, касающихся относительной эффективности различных ингибиторов и констант скоростей элементарных стадий реакций. [39]
Предполагая, что первая стадия - быстрая, а вторая - медленная, выведите уравнение для скорости образования устойчивой двойной спирали и выразите общую константу скорости реакции через константы скорости элементарных стадий. [40]
Таким образом, выбором константы гомогенного обрыва &10 удалось одновременно получить совпадающие с экспериментом границы полуострова распространения пламени и зависимость скорости пламени от давления и температуры, что свидетельствует о правильности выбора схемы и констант скоростей элементарных стадий реакции окисления сероуглерода. [41]
Заметим, что следует учитывать различие между мономолекулярной реакцией, которая включает простое химическое превращение на молекулярном уровне, и реакцией первого порядка, константа скорости которой может представлять собой сложную комбинацию констант равновесия и констант скоростей элементарных стадий. [42]
Заметим, что следует учитывать различие между мопомолекулярной реакцией, которая включает простое химическое превращение на молекулярном уровне, и реакцией первого порядка, константа скорости которой может представлять собой сложную комбинацию констант равновесия и констант скоростей элементарных стадий. [43]
Решение этой системы уравнений позволяет определить стационарные концентрации свободного фермента, субстрата и промежуточного соединения и при последующем использовании уравнения (5.2) найти значение наблюдаемой на опыте стационарной скорости реакции как функции исходных концентраций фермента, субстрата и констант скоростей элементарных стадий. [44]
Аналогичные данные по реакционной способности получены тем же способом для окисления, сульфирования, нитрования, алкилирования и других процессов, причем при разветвлении пути реакций на одной из быстрых элементарных стадий исследование состава продуктов является единственной возможностью определения отношения констант скоростей элементарных стадий. [45]
Страницы: 1 2 3 4