Константа - скорость - элементарная стадия
Cтраница 4
Однако определение констант скоростей элементарных стадий этих процессов встречает серьезную трудность - одним из реагентов являются промежуточные, как правило, гипотетические частицы ( например, NOj), концентрация которых неизвестна. [46]
Реакции электрофильного замещения в ароматическом ядре являются одним из важнейших классов реакций органической химии. Однако изучение констант скоростей элементарной стадии этих процессов упирается в серьезную трудность - одним из реагентов являются промежуточные, как правило, гипотетические частицы ( например, NO), концентрация которых неизвестна. Непосредственному измерению поддается лишь кинетика суммарного процесса, который является сложным. Поэтому данных об энергиях активации и стерических факторах элементарного акта электрофильного замещения не имеется. [47]
В ней рассмотрены методы численного интегрирования на ЭВМ уравнений химической кинетики для некоторых конкретных процессов. Значительный интерес представляет определение констант скоростей элементарных стадий и выбор наиболее вероятного механизма процесса. [48]
Реакция имеет первые порядки по катализатору и реагенту первой стадии, нулевой порядок по реагенту второй стадии и не тормозится веществом Z. Ее константа скорости равна константе скорости элементарной стадии образования промежуточного комплекса ( k), которую легко найти, разделив экспериментально найденную эффективную константу & Эф на концентрацию катализатора. [49]
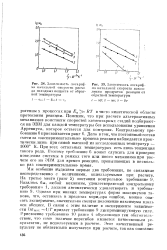 |
Зависимость логарпф - [ IMAGE ] Зашгашость логариф. [50] |
Поясним, что при расчете альтернативных механизмов константы скоростей элементарных стадий подбираются на ЭВМ для каждой температуры без использования уравнения Аррениуса, которое остается для контроля. Дело в том, что постоянный состав смеси за экспериментальные времена реакции наблюдается практически лишь при самой высокой из исследованных температур - 1000 К. [51]
Особый интерес представляет изучение медленных цепных процессов, обнаружение и идентификация свободных атомов и радикалов, определение их концентраций, вычисление констант скоростей элементарных стадий, установление связей между детальным механизмом процессов и их формально-кинетическими закономерностями. [52]
В этой главе мы обсудим кинетические закономерности реакции водорода с кислородом при высоких температурах и проследим их взаимосвязь с механизмом реакции при низких температурах. Именно с помощью метода ударной трубы удалось не только детально исследовать кинетический механизм быстрой реакции водорода с кислородом, но и количественно определить константы скоростей наиболее важных элементарных стадий. Сначала рассмотрим некоторые главные кинетические особенности быстрых цепных процессов при высоких температурах. Сравним метод ударной трубы с другими экспериментальными методами, обеспечивающими химиков важной количественной информацией о реакции водорода с кислородом. Рассмотрим различные методики регистрации в ударной трубе и информацию, получаемую с их помощью. Но основное внимание уделим последовательности элементарных стадий в полном механизме реакции водорода с кислородом и константам скоростей этих элементарных стадий. [53]
Голодец и Ройтер допускают существование эффективного псевдоравновесия активированного комплекса. Константа такого равновесия / Офф связана с константой скорости, находимой из эксперимента, так же, как и константа равновесия Кф связана с константой скорости элементарной стадии. [54]
Обычно кинетику химической реакции изучают в изотермических условиях, проводя эксперимент так, что эффекты саморазогрева незначительны ( интенсивный теплоотвод), а температура внешнего источника теплоты постоянна. За последние 15 лет развиты и все шире применяются разнообразные неизотермические методы изучения кинетики, которые позволяют получить кинетическое уравнение и энергию активации для брутто-процесса, в некоторых случаях измерить константы скорости элементарных стадий. [55]
Страницы: 1 2 3 4