Константа - трутон
Cтраница 3
Как видим, при кипении под атмосферным давлением отношение теплоты парообразования к абсолютной температуре, или приращение энтропии при кипении, есть величина постоянная. Эта постоянная называется константой Трутона. [31]
Таким образом, оказывается, что константа Трутона Д8 в случае фторуглеродов имеет нормальное значение. [32]
Константа Трутона для JF, равна 26 4 [7]; однако расчет этой величины основан на данных теплоты сублимации, а не теплоты испарения. Это дает основание считать, что истинное значение константы Трутона должно быть ниже. Таким образом, гептафторид иода ни в газообразном, ни в жидком состоянии не проявляет свойств ассоциированного соединения. [33]
Хлордифтор-амин, вероятно, в жидком виде не ассоциирован. Об этом можно судить, в частности, по константе Трутона ( 21 0), которая совпадает с теоретической величиной константы, характерной для недиссоциированных веществ. Поэтому для хлордифторамина наиболее характерной должна быть гомолитическая диссоциация связи IN - С1, а гетеролитическая диссоциация возможна лишь в особых случаях. В отличие от tNzFt, для которого гомолитическая диссоциация представляет собой равновесный процесс, диссоциация хлордифторамина по связи N - С1 имеет место, как правило, лишь при взаимодействии iNF2Cl с каким-либо веществом. [34]
Однако этот способ в общем оказался неудовлетворительным, потому что константа Трутона не одинакова для ассоциированных и неассоциированных жидкостей; кроме того, и степень ассоциации изменяется с температурой. [35]
Эти данные изображены на рис. 28.1 Е виде графика, соответствующего уравнению (28.27); теоретическое уравнение вполне удовлетворительно согласуется с якспеpit - ментальным и данными, за исключением системы ацетон - - метилацетат. Уравнение ( 28.27) следует считать полу: мпиричоским, так как яшдтюсттт с сильно различающимися константами Трутона вряд ли могут образовывать регулярные растворы. [36]
Это происходит оттого, что аммиак в отличие от своих аналогов в жидком состоянии в значительной степени ассоциирован. Что это действительно так, следует хотя бы из того, что аммиаку присуще аномально высокое значение константы Трутона ( см. стр. [37]
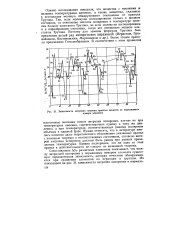 |
Зависимость энтропии кипения простых веществ от порядкового. [38] |
Однако исследования показали, что вещества с высокими и низкими температурами кипения, а также вещества, склонные к ассоциации молекул, обнаруживают отклонение от правила Трутона. Так, если молекулы ассоциированы только в жидком состоянии, то отношение теплоты испарения к температуре кипения больше константы Трутона, но если молекулы ассоциированы и в парообразном состоянии, тогда это отношение меньше константы Трутона. Более точное правило предложено Гильденбрандом. [39]
Скрытые теплоты испарения компонентов составляют: уксусной кислоты 96 75, этилацетата 87 5 и воды 540 кал / кг. Если принять, что в паровой фазе уксусная кислота присутствует в виде димеров с молекулярным весом 120, то константа Трутона для нее составит 29 6, что значительно ближе к значениям этих констант для этилацетата и воды. Соответственно с этим были пересчитаны данные о равновесии между жидкостью и паром. Исходя из приведенных в табл. 31 составов материальных по-токоз, было рассчитано изменение концентраций жидкости и пара на тарелках для бесконечного и нескольких конечных флегмовых чисел и на основании этого найдено необходимое число тарелок. [40]
Скрытые теплоты испарения компонентов составляют: уксусной кислоты 96 75, этилацетата 87 5 и воды 540 кал / кг. Если принять, что в паровой фазе уксусная кислота присутствует в виде димеров с молекулярным весом 120, то константа Трутона для нее составит 29 6, что значительно ближе к значениям этих констант для этилацетата и воды. Соответственно с этим были пересчитаны данные о равновесии между жидкостью и паром. Положение тарелки шитания определялось из условия ( 337), Исходя из приведенных в табл. 31 составов материальных потоков, бышо рассчитано изменение концентраций жидкости и пара на тарелках для - бесконечного и нескольких конечных флегмовых чисел и на основании этого найдено необходимое число тарелок. [41]
Другими критериями ассоциации в жидком состоянии являются константа Трутона и диэлектрическая постоянная жидкости. Величина ДЯ / Т для JF5 составляет 26 4 при температурах в интервале 30 - 60 С [46]; Руфф [17] приводит значение константы Трутона для JF5, равное 27 2, что характеризует пентафторид иода как ассоциированную жидкость. [42]
Однако исследования показали, что вещества с высокими и низкими температурами кипения, а также вещества, склонные к ассоциации молекул, обнаруживают отклонение от правила Трутона. Так, если молекулы ассоциированы только в жидком состоянии, то отношение теплоты испарения к температуре кипения больше константы Трутона, но если молекулы ассоциированы и в парообразном состоянии, тогда это отношение меньше константы Трутона. Более точное правило предложено Гильденбрандом. [43]
Лучше всего изучены пентафториды рутения и осмия. Элементарная ячейка этих двух веществ представляет собой тетрамер MtF20 [47, 54], в котором близкие к октаэдрическим группировки MFe соединены г ис-фторидными мостиками и образуют квадрат. Высокие значения констант Трутона указывают на значительную ассоциацию жидкости [28], однако природа паров неизвестна. Поскольку PtFB по своим физическим свойствам подобен [45] OsF5 и RuF5, постольку пентафторид платины может быть подобен этим пентафторидам и в структурном отношении. [44]
Очевидно, в дальнейшем усилия в изучении химии этих соединений будут направлены на синтез других представителей уже известных классов соединений и поиск новых. В частности, можно предположить, что в ближайшее время будут синтезированы комплексные соединения - производные пентафторида хлора. Довольно высокое значение константы Трутона пентафторида хлора ( 22 0) позволяет прогнозировать возможность его самоионизации в жидком состоянии, а следовательно, и образование комплексных соединений, содержащих соответствующие ионы. [45]
Страницы: 1 2 3 4